Эпидемиология и Инфекционные болезни. Актуальные вопросы №5 / 2013
Оптимизация лабораторной составляющей диагностической подсистемы эпидемиологического надзора за аскаридозной инвазией
Башкирский государственный медицинский университет Минздрава России, Уфа; Республиканская детская клиническая больница, Уфа
Цель исследования. Изучение эпидемиологических проявлений аскаридоза для обоснования групп обследуемых больных и оценки эффективности метода полимеразной цепной реакции (ПЦР) в сравнении с традиционной микроскопией.
Материалы и методы. Для оценки информативности указанных методов в период 2009–2012 гг. были обследованы 209 пациентов с кишечной стадией аскаридоза и 80 здоровых лиц.
Результаты. Основной группой риска по заболеваемости аскаридозом являлются дети в возрасте 1–6 лет. В этой группе больных были получены наиболее адекватные результаты, доказывающие, что ПЦР имеет более высокую чувствительность, специфичность и диагностическую эффективность, чем микроскопический метод.
Заключение. Для оптимизации диагностической подсистемы эпидемиологического надзора за аскаридозной инвазией необходимо широко внедрять молекулярно-генетические методы исследования в практическое здравоохранение при диагностике гельминтозов.
Эффективность эпидемиологического надзора за любой патологией, в том числе аскаридозной инвазией, во многом определяется информативностью диагностической подсистемы, важным компонентом которой является детекция этиологического агента. При аскаридозе основным методом лабораторной диагностики является обнаружение яиц гельминта в фекалиях с использованием методов Като и Миура, методов обогащения по Фюллеборну, Калантарян или Красильникову [1, 2]. Наличие в кишечнике аскарид не всегда сопровождается обнаружением их яиц в фекалиях человека, например, при паразитировании особей одного пола (3–5%), неполовозрелых или старых самок [3]. Эти данные указывают на недостаточную чувствительность используемых методов диагностики и низкую интенсивность регистрируемой заболеваемости аскаридозом, составляющей в России от 40 до 60 тыс. случаев в год, что равно 15% от общего числа больных гельминтозами [4, 5].
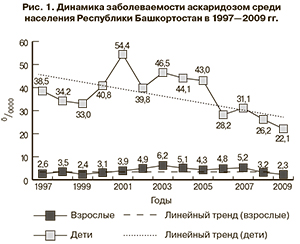 Повсеместное снижение заболеваемости аскаридозом в последнее десятилетие связано не только с низким качеством лабораторной диагностики этой инвазии, но во многом и с существенным сокращением обследования населения на паразитозы в целом [5–8]. В действительности же, по экспертным оценкам, заболеваемость паразитозами в нашей стране может достигать 20 млн случаев [9]. О возможности развития такого сценария при гельминтозах свидетельствует регистрируемая тенденция роста гастроэнтерологических и аллергических заболеваний у детей, в определенной степени обусловленных Ascaris lumbricoides [10]. На это указывают результаты выборочных исследований, проведенных с использованием общепринятых рутинных методов, согласно которым выявляемость данного гельминта может составлять более 350 тыс. случаев в год [11]. При этом не исключается возможность инфицирования людей свиной аскаридой – Ascaris suum [12, 13]. Прогностические ожидания в отношении этой инвазии при существующем уровне лабораторной диагностики являются неутешительными, поскольку ареал ее распространения постоянно расширяется, во многом соответствуя социально-экономическому статусу и природным условиям конкретного региона [14]. Знание истинных масштабов ее распространения в отдельных регионах, в частности в Республике Башкортостан, требует использования высокочувствительных и специфичных молекулярно-генетических методов диагностики аскаридоза для последующего совершенствования на этой основе регионального компонента ...
Повсеместное снижение заболеваемости аскаридозом в последнее десятилетие связано не только с низким качеством лабораторной диагностики этой инвазии, но во многом и с существенным сокращением обследования населения на паразитозы в целом [5–8]. В действительности же, по экспертным оценкам, заболеваемость паразитозами в нашей стране может достигать 20 млн случаев [9]. О возможности развития такого сценария при гельминтозах свидетельствует регистрируемая тенденция роста гастроэнтерологических и аллергических заболеваний у детей, в определенной степени обусловленных Ascaris lumbricoides [10]. На это указывают результаты выборочных исследований, проведенных с использованием общепринятых рутинных методов, согласно которым выявляемость данного гельминта может составлять более 350 тыс. случаев в год [11]. При этом не исключается возможность инфицирования людей свиной аскаридой – Ascaris suum [12, 13]. Прогностические ожидания в отношении этой инвазии при существующем уровне лабораторной диагностики являются неутешительными, поскольку ареал ее распространения постоянно расширяется, во многом соответствуя социально-экономическому статусу и природным условиям конкретного региона [14]. Знание истинных масштабов ее распространения в отдельных регионах, в частности в Республике Башкортостан, требует использования высокочувствительных и специфичных молекулярно-генетических методов диагностики аскаридоза для последующего совершенствования на этой основе регионального компонента ...












