Фарматека №7 (360) / 2018
Опыт персонализированного назначения неоадъювантной химиотерапии больным раком молочной железы: проспективное исследование
1 НИИ онкологии Томского Национального исследовательского медицинского центра Российской академии наук, Томск, Россия;
2 Сибирский Государственный медицинский университет, Томск, Россия;
3 Национальный исследовательский Томский Государственный университет, Томск, Россия
Одной из наиболее значимых причин невысокой эффективности неоадъювантной химиотерапии (НАХТ) рака молочной железы (РМЖ) является отсутствие персонализированного подхода к выбору схем конвенциональной химиотерапии.
Цель исследования. Разработка и проспективная клиническая апробация алгоритма персонализированного назначения НАХТ больным РМЖ с использованием молекулярно-генетических маркеров опухоли. Методы. Все пациентки, участвовавшие в исследовании, были разделены на две группы. В первую (исследовательскую) группу вошли 37 больных РМЖ. До начала лечения из опухолевой ткани этих пациенток, полученной при биопсии, выделили ДНК и РНК при помощи микроматрицы CytoScan HD Array (Affymetrix, США), количественной ПЦР определили копийность и уровень экспрессии генов АВС-транспортеров и генов чувствительности BRCA1, Top2a, TYMS и TUBB3. По результатам молекулярно-генетического анализа для пациенток персонализированно определили тактику лечения. Во вторую (исторический контроль) группу была включена 71 пациентка с люминальным В HER2(-) РМЖ, которым НАХТ проведена без учета молекулярно-генетических характеристик опухоли. Результаты. В исследование были включены 108 больных люминальным В HER2(-)-РМЖ. Разработан двухуровневый алгоритм персонализированного назначения НАХТ. На первом уровне, исходя из маркеров копийности генов АВС и регионов 18р11.1-32; 11q21- 25 и 1q21.3-44, определена целесообразность проведения предоперационного лечения, на втором в случае положительного ответа осуществлялся персонализированный выбор схемы на основании маркеров копийности и экспрессии генов чувствительности. Персонализированная НАХТ была назначена 26 из 37 больных, 11 пациенток начали лечение с операции, поскольку показания к проведению химиотерапии в предоперационном периоде у них отсутствовали. Непосредственная эффективность НАХТ в исследовательской группе составила 88,5% (23 из 26), стабилизация наблюдалась у 3 (11,5%) больных. В контрольной группе непосредственная эффективность НАХТ составила 53,5% (38 из 71), стабилизация и прогрессирование имели место у 46,5% (33 из 71) больных. Различия между группами оказались статистически значимыми (р=0,002). Заключение. Определены новые информативные предсказательные критерии, использование которых существенно повысило эффективность НАХТ по сравнению со стандартными подходами к назначению предоперационного лечения.
ВВЕДЕНИЕ
Рак молочной железы (РМЖ) на протяжении многих лет занимает лидирующие позиции по показателям заболеваемости и смертности среди женского населения как в мире, так и в России [1, 2]. Это гетерогенное заболевание, включающее пять основных молекулярных подтипов, характеризующихся различными особенностями клинического течения, прогноза заболевания, что наряду с оценкой распространенности опухолевого процесса в значительной мере определяет выбор и объем комбинированного лечения [3]. Более чем для половины больных одной из основных терапевтических опций является системная химиотерапия (ХТ) – это больные, которым диагностируется люминальный В, трижды негативный и HER-позитивный типы опухоли [3]. В настоящее время цитостатическая терапия активно используется в предоперационном режиме [4], что обусловлено возможностью достижения полного морфологического регресса (ПМР) опухоли, ассоциированного с улучшением отдаленных результатов [5]; стремлением к уменьшению объема первичной опухоли; созданию более благоприятных условий для выполнения органосохраняющих операций [4], а также определением чувствительности первичной опухоли к проводимой ХТ in vivo, позволяя на этом основании планировать лечение в адъювантном режиме.
Однако далеко не всегда при проведении неоадъювантной ХТ (НАХТ) мы получаем ожидаемые результаты. Причин, определяющих низкую эффективность системного лечения больных со злокачественными новообразованиями, достаточно много. Одной из наиболее значимых является отсутствие персонализированного подхода к выбору схем цитостатических препаратов при проведении конвенциональной ХТ. Индивидуализация лечения может быть основана на определении молекулярно-генетических маркеров опухоли, которые служат мишенью действия отдельных препаратов и определяют чувствительность новообразования к ним – генов чувствительности [6, 7], а также маркеров, ассоциированных с неспецифической резистентностью к ХТ – генов множественной лекарственной устойчивости (МЛУ) [8].
Анализ данных литературы и собственных результатов дает основание полагать, что и гены химиочувствительности, и гены МЛУ могут рассматриваться в качестве информативных предсказательных критериев [7, 9, 10]. При наличии клинических показаний к проведению системной ХТ больным РМЖ в неоадъювантном режиме они позволят ответить на два основных вопроса: следует ли ожидать эффекта от планируемой цитостатической терапии и если да, то какие препараты (схемы) необходимо при этом использовать?
Целью нашего исследования стали разработка и проспективная клиническая апробация алгоритма персонализированного назначения НАХТ больным люминальным В HER2(-)-РМЖ с использованием молекулярно-генетических маркеров опухоли.
МЕТОДЫ
Всего в исследование были включены 108 больных операбельным люминальным В HER2(-)-РМЖ. На этапе диагностики всем больным проведено полное клинико-инструментальное обследование, объем которого соответствовал алгоритмам, рекомендованным и утвержденным Минздравом РФ.
Согласно дизайну исследования, больные были разделены на две группы (рис. 1). По основным клинико-морфологическим характеристикам группы были сопоставимыми: у большей части пациенток распространенность процесса оценивалась как IIA–IIB-стадии. Возраст больных варьировался от 22 до 68 лет (в среднем по группам он составил 47 и 48 лет). Опухоли в молочной железе преимущественно были представлены инвазивной карциномой неспецифического типа 2-й степени злокачественности.
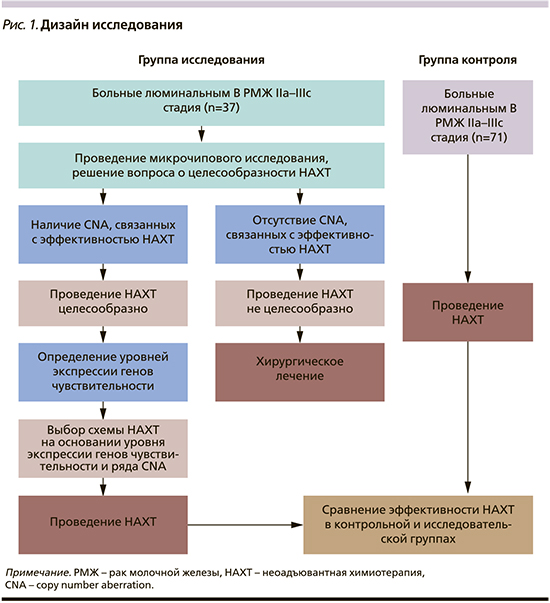
В первую (исследовательскую) группу вошли 37 больных РМЖ. До начала лечения из опухолевой ткани этих пациенток, полученной при биопсии новообразования, выделяли ДНК и РНК. ДНК опухоли использовали для микрочипового исследования на микроматрице CytoScan HD Array (Affymetrix, США). Были определены CNA-маркеры, сопряженные с эффективностью предоперационной ХТ, и копийность локусов генов чувствительности к отдельным препаратам. Если в опухолевой ткани они отсутствовали, первым этапом комбинированного лечения было выполнение радикального оперативного вмешательства. При идентификации маркеров, сопряженных с высокой эффективностью НАХТ, дополнительно к копийности некоторых генов чувствительности (Top2a, TYMS и TUBB3) определяли и уровни их экспрессии, используя РНК опухолевой ткани. Далее по совокупности полученных данных осуществлен выбор схемы лечения. Больным, которым была показана предоперационная ХТ, она назначалась в зависимости от молекулярно-генетических характеристик опухоли по схемам: FAC (5-фторурацил, доксорубицин,












