Фарматека №8 (341) / 2017
Опыт применения комбинации дабрафениба и траметиниба у больных метастатической меланомой кожи в условиях реальной клинической практики в России
ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России, Москва
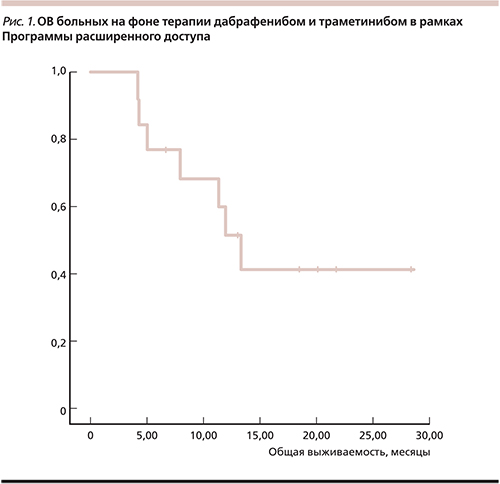
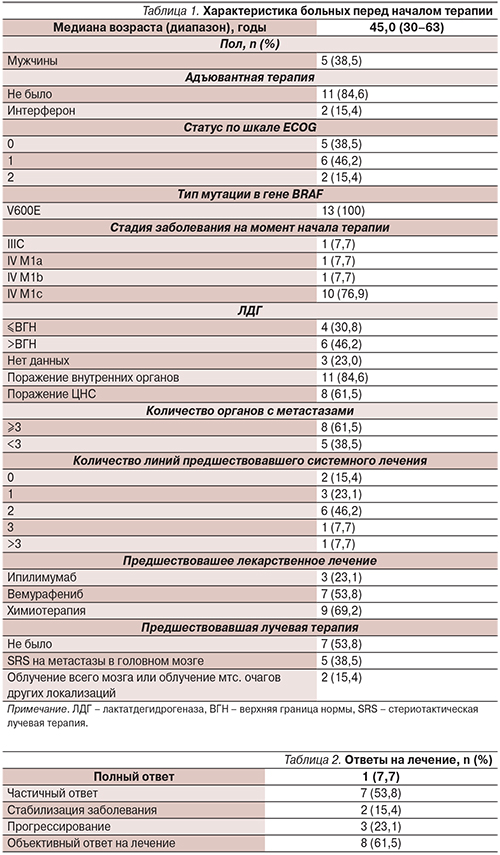
За последние 5 лет терапия метастатической и нерезектбаельной меланомы претерпела существенные изменения. В крупных клинических исследованиях новые лекарственные препараты демонстрируют высокую эффективность. Проанализирован опыт применения комбинации дабрафениба и траметиниба в рамках Программы расширенного доступа к этим препаратам в России. В период с марта 2015 по июнь 2015 г. в программу были включены 14 больных. Медиана их возраста составила 45 лет (диапазон – 30–63), мужчин было 38,5%, у всех пациентов в опухоли обнаружена мутация BRAF V600E. Статус по шкале ECOG 0-1 был у 84,6%, распространенность болезни, соответствующая M1c, определена у 76,9% больных. Уровень лактатдегидрогеназы выше верхней границы нормы был у 46,2% пациентов. Две и более линий предшествовавшей терапии получили 53,8% больных. Частота объективных ответов на лечение составила 61,5%, стабилизации – 15,4%, прогрессирования – 23,1%. Медиана выживаемости без прогрессирования составила 7,29 месяца (95% ДИ – 3,74–10,84), двухлетняя выживаемость без прогрессирования – 22%. Медиана общей выживаемости составила 13,27 месяца (95% ДИ – 10,3–16,2 месяца), двухлетняя общая выживаемость – 43%. В ходе исследования не было отмечено серьезных нежелательных явлений, связанных с приемом препаратов. Также не было выявлено новых нежелательных явлений. Сделан вывод, согласно которому комбинация ингибиторов BRAF и МЕК – дабрафениба и траметиниба – представляет собой высокоэффективный и хорошо переносимый вариант лечения метастатической или нерезектабельной меланомы с мутацией в гене BRAF V600 в первой и последующих линиях терапии. Данные упомянутой программы расширенного доступа согласуются с результатами ранее проведенных рандомизированных
исследований.
Введение
Лечение больных метастатической меланомой остается непростой задачей, несмотря на впечатляющие достижения лекарственной терапии. Результаты недавно проведенных клинических исследований демонстрируют почти двукратное увеличение общей выживаемости (ОВ) и выживаемости без прогрессирования (ВБП) при использовании как лекарственных препаратов, действующих на опухоли с мутацией в гене BRAF [1–4], так и модуляторов иммунологического синапса, в т.ч. больными без мутации в гене BRAF [5–8].
Эффективность терапии, направленной против опухоли с мутацией в гене BRAF, по данным клинических исследований, оказывается весьма высокой в первой линии лечения и несколько снижается при использовании этих лекарственных средств во второй и последующих линиях терапии [2].
Однако в реальной клинической практике в РФ пациенты, как правило, не получают наиболее эффективного лечения в первой линии терапии. В данной работе мы провели анализ эффективности и переносимости терапии комбинацией ингибитора BRAF, дабрафениба, и ингибитора МЕК, траметиниба, пациентами с метастатической меланомой, принимавшими участие в Программе расширенного доступа к препаратам в отделении биотерапии опухолей РОНЦ им. Н.Н. Блохина Минздрава России.
Пациенты и методы
Критерии включения и невключения в программу
Основные критерии для участия пациентов в программе: возраст старше 18 лет, добровольное информированное согласие, наличие мутации в гене BRAF (независимо от ее типа), способность принимать пероральные лекарственные препараты, общее состояние по шкале ECOG от 0 до 3, стабильное клиническое состояние, адекватная контрацепция для женщин детородного возраста.
Основные критерии невключения пациентов в программу: беременность или кормление грудью, необходимость проведения другого противоопухолевого лечения, наличие другой (второй) злокачественной опухоли, выявленной в течение года или позднее до планируемого включения в программу, в которой возможна активация сигнального пути RAS (специального тестирования на мутацию в гене RAS проводить не требовалось).
Следует отметить, что к участию в программе допускали пациентов, ранее получавших ингибиторы BRAF или МЕК (кроме дабрафениба и траметиниба) и не имевших признаков прогрессирования на фоне их приема (т.е. предшествовавшее лечение ингибиторами BRAF или МЕК могло быть прекращено по причине непереносимости, отсутствия доступа к препарату или случаев прогрессирования, когда новые очаги поражают исключительно ЦНС).
К участию в программе не допускали лиц с известной аллергией на компоненты препарата (например, ДМСО), высоким риском окклюзии вен сетчатки, острым коронарным синдромом или застойной сердечной недостаточностью 3-го и 4-го функциональных классов по классификации Нью-Йоркской ассоциации сердца (NYHA).
Исследуемый препарат и ход лечения
Препараты для Программы расширенного доступа были любезно предоставлены компанией ГлаксоСмитКляйн, далее по ходу продолжения программы дополнительные поставки препаратов осуществлены компанией Новаритс, к которой в тот период времени перешли права на регистрационные свидетельства дабрафениба и траметиниба.
Пациентам, удовлетворявшим критериям включения и не имевшим критериев исключения, выдавали препарат дабрафениб, который следовало принимать в дозе 150 мг (две капсулы по 75 мг) внутрь 2 раза в сутки, и траметиниб, который следовало принимать по 1 таблетке (2 мг) 1 раз в сутки.
Лечение продолжалось до непереносимости терапии, не купируемой снижением дозы, или до прогрессирования заболевания. При этом допускалось продолжение терапии после наступления прогрессирования в случае, если врач-исследователь видел в этом пользу.
Оценку эффекта терапии проводили каждые 2–3 месяца. Для оценки эффекта использованы критерии RECIST 1.1 [9].
Статистический анализ
Перед началом программы никакого статистического анализа не было запланировано. Для описания характеристик ...












