Клиническая Нефрология №1 / 2025
Перспективы фармакотерапии анемии с помощью ингибиторов HIF-пролилгидроксилазы у пациентов с хронической болезнью почек
1) ФГБОУ ВО «Смоленский государственный медицинский университет» Минздрава РФ, Смоленск, Россия;
2) Санкт-Петербургский государственный университет, Санкт-Петербург, Россия
Анемия является частым осложнением хронической болезни почек (ХБП) и вызвана дефицитом эндогенного эритропоэтина (EPO) и железа. Ингибиторы пролилгидроксилазы фактора, индуцируемого гипоксией (HIF), представляют собой новый класс препаратов для лечения анемии при ХБП. Наряду с препаратами железа и эритропоэз-стимулирующими препаратами (ЭСП) ингибиторы HIF-пролилгидроксилазы (HIF-PHI) могут занять свое место в коррекции анемии для снижения потребности в гемотрансфузии у пациентов и демонстрируют не меньшую, чем ЭСП, эффективность. В отличие от последних HIF-PHI являются пероральными препаратами, повышающими уровень эндогенного EPO, снижающими уровень гепсидина и улучшающими гомеостаз железа. Однако способность препаратов этой группы за счет стабилизации транскрипционного фактора HIF увеличивать экспрессию целого ряда HIF-ассоциированных генов, не только EPO и белков, участвующих в обмене железа, приводит к неизбирательности их действия. Особое опасение вызывает активация ангиогенеза, связанная с усилением образования фактора роста эндотелия сосудов (VEGF), что может стимулировать рост опухоли, повышать риск метастазов, быть связано с плохим прогнозом, лекарственной устойчивостью при различных видах злокачественных новообразований, а также влиять на прогрессирование поликистозной болезни почек и диабетической ретинопатии. Кроме того, отмечается повышенный риск тромбообразования, гиперкалиемии, нарушений функции щитовидной железы и др. Все это диктует необходимость проведения анализа соотношения польза-риск при выборе HIF-PHI в качестве противоанемических средств и долгосрочных клинических исследований препаратов этой группы для оценки их безопасности.
Введение
Понимание процессов кислородзависимой регуляции эритропоэза и связи между гипоксией индуцированным фактором (HIF), эритропоэтином (EPO), содержанием железа и хроническим воспалением послужило основанием для появления в клинике ингибиторов HIF пролилгидроксилазы (HIF-PHI) для лечения анемии у пациентов с хронической болезнью почек (ХБП) [1–3]. HIF-PHI по сравнению с рекомбинантными препаратами EPO обладают принципиально иным механизмом действия. Если эритропоэз-стимулирующие препараты (ЭСП) в ситуации прогрессирующего дефицита эндогенного EPO при ХБП стимулируют эритропоэтиновые рецепторы, прежде всего на клетках – предшественниках эритроцитов в костном мозге, то препараты новой группы обладают ферментным механизмом действия, блокируя фермент HIF-пролилгидроксилазу. Это приводит к стабилизации HIF и повышению экспрессии генов, которые обеспечивают адаптацию клетки к гипоксии и стимулируют эритропоэз (гены EPO), ангиогенез (ген фактора роста эндотелия сосудов – VEGF), ферменты гликолиза (ген альдолазы, лактатдегидрогеназы, фосфофруктокиназы, пируваткиназы и др.). Кроме того, HIF-1 регулирует экспрессию генов, участвующих в обмене железа, регуляции сосудистого тонуса, клеточной пролиферации, апоптоза, липогенеза, свертывании крови, формировании лекарственной устойчивости и др. [2, 4, 5].
HIF-PHI применяются перорально, их противоанемическая эффективность, по результатам большинства многочисленных рандомизированных контролируемых клинических исследований (РКИ) [6], а также по проведенным на их основе систематическим обзорам и метаанализам [7, 8], не уступает эффективности ЭСП [9], а иногда даже превосходит [10, 11]. Международные непантетованные названия препаратов объединяют их в группу «дустаты», среди которых на мировом рынке представлено 6 HIF-PHI: вададустат, дапродустат, дезидустат, молидустат, роксадустат и энародустат. В России с 2022 г. зарегистрирован только роксадустат, который с 2024 г. включен в перечень жизненно необходимых и важнейших лекарственных препаратов. Несмотря на эффективное повышение уровня гемоглобина (Hb) с помощью «дустатов» как у пациентов на преддиализных стадиях ХБП, так и находящихся на диализе, оценка их безопасности, особенно в случае длительного использования, остается актуальной задачей, прежде всего из-за потенциального проангиогенного и проонкогенного действий HIF-PHI, риска тромбозов и сердечно-сосудистых осложнений, а также метаболических нарушений.
Цель обзора: оценка эффективности и безопасности HIF-PHI на основе анализа экспериментальных и клинических исследований.
Гипоксией индуцированный фактор
Одним из способов стабилизации HIF является ингибирование фермента – HIF-пролилгидроксилазы (PH). В условиях нормоксии этот фермент отвечает за гидроксилирование остатков пролина HIF-α, в результате чего α-субъединица подвергается протеасомной деградации. Специфическое ингибирование пролилгидроксилазы путем связывания с активными центрами фермента приводит, как и в случае воздействия гипоксии, к стабилизации HIF-α, объединению с субъединицей HIF-β, переходу HIF из цитоплазмы в ядро клетки, связыванию с определенными последовательностями ДНК и увеличению экспрессии генов, вовлеченных в противогипоксическую защиту и изменение энергетического метаболизма [2, 12]. Происходит повышение интенсивности синтеза ферментов гликолиза, экспрессии мембранных транспортеров глюкозы, генов EPO, фактора роста эндотелия сосудов (VEGF), генов митохондрий, вовлеченных в использование энергии, генов, участвующих в обмене железа, регуляции сосудистого тонуса, клеточной пролиферации, апоптоза, выживаемости клеток, лекарственной устойчивости, коагуляции и активации тромбоцитов и др. (рисунок).
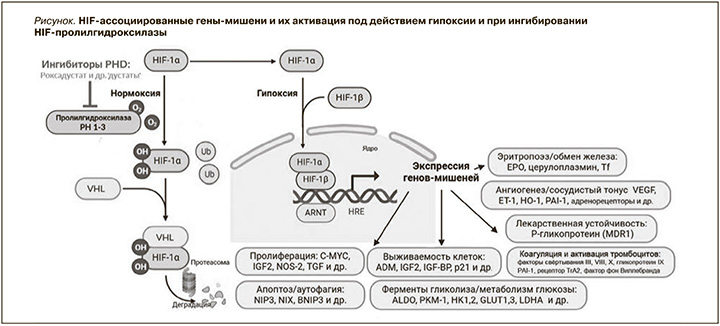
Эффективность HIF-PHI (дустатов)
Одним из первых низкомолекулярных HIF-PHI, используемых перорально (70 мг/доза) трижды в неделю для лечения анемии у пациентов с ХБП, находящихся на диализе, был внедрен роксадустат [13]. Препарат обратимо связывается и ингибирует фермент HIF-пролилгидроксилазу, блокируя деградацию α-субъединицы HIF и способствуя повышению активности HIF, что приводит к увеличению выработки эндогенного EPO и усилению эритропоэза. Роксадустат также повышает активность белков – переносчиков железа (трансферрина, переносчика двухвалентных металлов 1), уровень церулоплазмина. Важно, что роксадустат снижает экспрессию гепсидина – белка-регулятора концентрации железа, уровень которого повышается при воспалении во время ХБП и нарушает всасывание железа через его экспорт ферропортином из энтероцитов в кровь [14]. В результате действия роксадустата улучшается биодоступность железа, повышается поступление железа из ретикулоэндотелиальных макрофагов и гепатоцитов в плазму, что способствует доступности железа для кроветворения [15]. В итоге увеличивается выработка Hb и повышается число эритроцитов. Также действуют и другие препараты HIF-PHI, имеющиеся на мир...












