Акушерство и Гинекология №12 / 2022
Перспективы применения экзомного секвенирования для решения проблем в репродукции человека (часть I)
1) ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта», Санкт-Петербург, Россия;
2) ФГБУ «Детский научно-клинический центр инфекционных болезней Федерального медико-биологического агентства», Санкт-Петербург, Россия
Появление новых генетических технологий является ключевым аспектом прогресса в развитии молекулярной медицины. Благодаря им существенно расширяются возможности генетических лабораторных тестов в клинической практике, происходят изменения в терминологии. Наметился четкий переход от изучения индивидуальных генов и их вариантов (мутаций) к исследованиям экзома для анализа патогеномики, поиску биомаркеров, досимптоматической профилактике и персонализированному лечению различных заболеваний человека. В обзоре (часть 1) представлены собственные и литературные данные о применении технологии NGS, экзомном секвенировании, генетическом и клиническом генетическом паспорте, сложностях, особенностях и перспективах внедрения новых подходов в практическую медицину.
Заключение: Разработка научных основ точной медицины для изучения, диагностики и лечения моногенных болезней, а также олигогенных, мультифакториальных и инфекционных заболеваний будет определяться эффективностью использования NGS-технологий с учетом современных алгоритмов анализа и классических генетических понятий экспрессивности и пенетрантности.
Научно-технический прогресс в биологии и медицине в конце ХХ и начале ХХI вв. привел к появлению новых высокотехнологичных методов ранней диагностики. Это способствовало выявлению причин редких моногенных заболеваний, улучшению профилактики и повышению эффективности лечения многофакторных социально-значимых заболеваний [1].
Создание технологии секвенирования позволило расшифровать последовательность генома человека. С этой целью в 1990 г. Национальным Институтом здоровья США был запущен проект «Геном человека» (The Human Genome Project, HGP), в котором помимо США участвовали Великобритания, Япония, Франция, Германия, Испания и Китай. Проект завершился в 2003 г., когда Национальным центром биотехнологической информации США (NCBI) была опубликована законченная версия сборки генома человека (hg17) [2]. Однако, и данная версия сборки содержала пропуски в последовательности ДНК, которые были впоследствии ликвидированы. Последняя текущая версия генома человека GRCh38.p14 опубликована Консорциумом исследований генома (GRC) 9 мая 2022 г. [3].
Важно отметить, что удельный вклад одного и того же генетического полиморфизма в этиологию и патогенез любого заболевания в разных популяциях и этнических группах может различаться [4, 5]. Поэтому одним из ключевых направлений повышения качества генетической диагностики, основанной на экзомном секвенировании и клиническом генетическом паспорте, является развитие, прежде всего, популяционных баз данных аллельных частот генетических вариантов (в том числе отечественных), играющих роль в патогенезе наследственных и мультифакториальных заболеваний (МФЗ), совершенствование биоинформатических и статистических протоколов обработки и анализа данных секвенирования, особенно в плохо изученных популяциях [6].
Преимущества и недостатки различных технологий NGS
Технологию NGS (Next Generation Sequencing – секвенирование нового поколения) можно разделить на секвенирование c короткими (от 100 до 600 пар нуклеотидов) и длинными (до 900 КБ) прочтениями. В настоящее время наиболее часто применяются методы с короткими прочтениями последовательностей, поскольку они дешевле и имеют более высокую точность, чем методы с длинными прочтениями. Однако это не всегда так. В частности, нами было показано, что при большом покрытии (около 4000Х) применимость данных секвенирования нанопор для определения вариантов митохондриального генома полностью согласуется с данными, полученными на секвенаторах фирмы Illumina [7]. При этом технологии с короткими прочтениями не могут использоваться для секвенирования повторяющихся или гетерозиготных последовательностей, для которых применяются технологии секвенирования с длинными прочтениями [8]. Особенности различных применяемых в медицинской практике технологий NGS представлены в таблице.
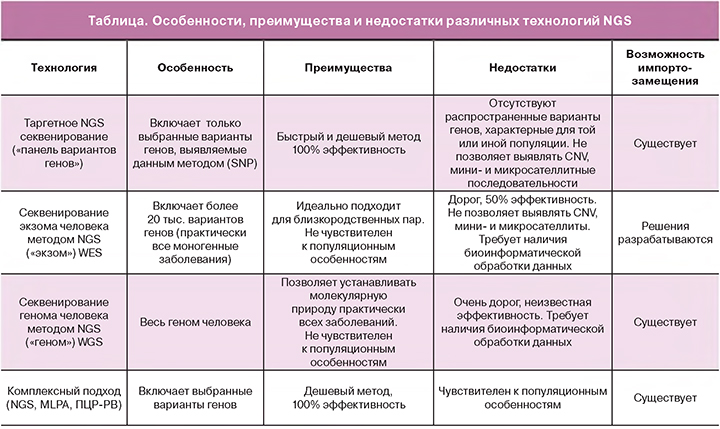
Таргетное секвенирование стало одним из первых практических приложений NGS. Благодаря этой технологии стало возможным прочитывать отдельные гены в 1000 раз дешевле, чем ранее, с использованием полимеразной цепной реакции для длинных фрагментов, позволяющей амплифицировать участки до 50–100000 пар оснований. Данный подход особенно эффективен для анализа небольших генов [9, 10]. Полногеномное секвенирование не так распространено в практике, хотя позволяет провести полный анализ всех генов человека...












