Фарматека №7 / 2021
Поиск новых прогностических и предиктивных маркеров чувствительности к эндокринотерапии, химиотерапии и иммунотерапии рака молочной железы
1) Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова, Санкт-Петербург, Россия;
2) Северо-Западный государственный медицинский университет им. И. И. Мечникова, Санкт-Петербург, Россия;
3) Первый Санкт-Петербургский государственный медицинский университет им. И.П. Павлова, Санкт-Петербург, Россия
Наблюдающееся в последние годы снижение смертности от рака молочной железы (РМЖ) в Европе, Северной Америке и в в России в большей степени связано с более широким применением неоадъювантной и адъювантной системной терапии, включая эндокринотерапию (ЭТ), химиотерапию (ХТ), таргетную и иммунотерапию. Планирование системной терапии только на основании стадии, возраста и патоморфологии (гистологический тип и степень злокачественности) представляется недостаточным. Необходимы более точные прогностические и предиктивные маркеры чувствительности к применяемым и новым видам лекарственных препаратов. В последнее время считается, что экспрессия ER от 1 до 10% служит основанием назначения ЭТ. На 12-й конференции EBCC заявлено о нецелесообразности применения адъювантной ХТ в отношении большинства пациентов с люминальным А-подтипом РМЖ и метастатическими лимфоузлами. Вместе с тем известно, что у значительного числа пациентов с ER+ РМЖ возникает поздний (отсроченный) рецидив через 5 и более лет после операции. Как предотвратить развитие резистентности к эндокринотерапии (ЭТ)? Многие маркеры резистентности уже известны. Наиболее исследованы ингибиторы CDK 4/6 (палбоциклиб, абемациклиб, рибоциклиб). Доказана их высокая эффективность при метастатических ER+ РМЖ. Промежуточная оценка адъювантного применения ингибиторов CDK 4/6 показала противоречивые результаты: достоверное улучшение 2-летней DFS в испытании MonarchE и негативные результаты в испытании PALLAS. В испытании MonarchE включались пациенты с операбельным РМЖ высокого риска. Кроме того, средние сроки наблюдения (от 15 до 28 месяцев) недостаточны для окончательного заключения об эффективности адъювантного лечения. У женщин с остаточным инвазивным HER2- позитивным РМЖ после неоадъювантной системной терапии (НСТ) адъювантная терапия трастузумаб-эмтанзином (TD-M) значительно снижает риск рецидива. Пациенты с резидуальным трижды негативным РМЖ (ТНРМЖ) получают выгоду от постнеоадъювантной терапии капецитабином. Прогностические биомаркеры (TILs, PD1, лиганда PDL1) являются главным регулятором иммунного ответа на растущую опухоль. В последние годы были разработаны моноклональные антитела, блокирующие иммунные «чекпоинт-белки». При РМЖ наиболее исследован препарат атезолизумаб (анти-PDL1-антитело). В исследовании Impassion-130 использование атезолизумаба (ингибитора лиганда PDL1) в комбинации с наб-паклитакселом при метастатическом ТНРМЖ увеличило показатели 2-летней беспрогрессивной выживаемости (в группе с позитивным PDL1). В испытании NeoTrip PDL1 показано, что комбинация атезолизумаба, карбоплатина и наб-паклитаксела увеличивает частоту достижения pCR на 10% и более.
Актуальность
Тридцать–сорок лет назад, когда в большинстве стран в основном выполнялась радикальная мастэктомия, увеличение показателей выживаемости и определенное снижение смертности в некоторых странах Европы и Северной Америки связывали с внедрением маммографического скрининга. В последующие годы по мере лучшего понимания механизма и биологии заболевания, обусловившего более широкое применение адъювантной системной терапии (гормоно- и химиотерапии), наблюдающееся увеличение показателей выживаемости нельзя было объяснить влиянием только скрининга, т.к. оно наблюдалось и вне скрининга (при более распространенных карциномах молочной железы) [1, 2].
В практических условиях планирование системного лечения основывается на стадии, иммуногистохимическом подтипе заболевания и возра-сте пациента (пре-, постменопауза). Соответственно, выделяются люминальные (ER+) опухоли (люминальный А и люминальный B), HER2-позитивные и трижды негативные подтипы (фенотипы) РМЖ (ТНРМЖ). Они не полностью соответствуют молекулярно-генетическим вариантам, определяемым по экспрессии соответствующих генов (например, с помощью РАМ-50) [3, 4].
В рекомендациях St. Gallen (2019) H.J. Bustein [5] и ESMO (European Society of Medical Oncology, 2019, 2020) [6] уровень экспрессии рецепторов эстрогенов (ER) от 1 до 10%, ранее считавшийся низким для назначения гормонотерапии, был признан достаточным обоснованием гормонального лечения. Конечно, это вызывает много вопросов, т.к. до сих пор не проводилось специальных клинических испытаний эффективности ЭТ при низкой экспрессии ER (от 1 до 10%) [7].
Сторонники такой широкой интерпретации позитивности ER напоминают, что в 2018–2019 гг. произошел очередной пересмотр методологии лабораторного определения и трактовки позитивности экспрессии рецепторов стероидных гормонов. Если принять эту точку зрения, то 70–80% РМЖ следует считать гормонзависимыми при уровне экспрессии ER выше 1%.
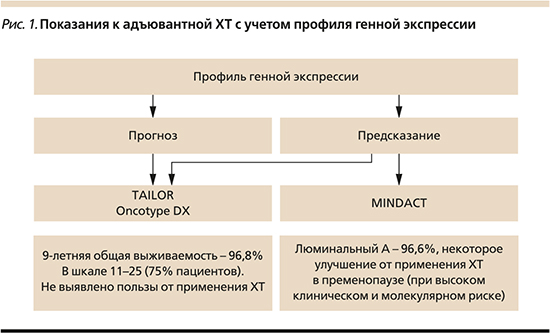
В связи с широким распространением люминального А – раннего (операбельного) РМЖ, важно знать, какие из этих пациентов нуждаются кроме ЭТ в адъювантной или неоадъювантной химиотерапии (ХТ). На прошедшей в октябре 2020 г. 12-й конференции по раннему РМЖ (EBCC-12, Barcelona, 2020) по крайней мере две сессии были посвящены лечению люминальных опухолей молочной железы. Одна из них называлась «Пациенты с люминальным А-подтипом РМЖ не нуждаются в адъювантной ХТ» (председатель – д-р Christos Sotiriou). Показания к адъювантной ХТ были рассмотрены с учетом профиля генной экспрессии (рис. 1). Еще на конференции St. Gallen (2019) на вопрос, полезен ли геномный анализ в определении показаний к ХТ при ER+ РМЖ, Т3N0 или 1–3 N+» 74,5% членов панели экспертов ответили позитивно. На 12-й конференции EBCC (2020) были рассмотрены 9-летние результаты двух крупнейших клинических испытаний (TAILOR – генная экспрессия ONCOTYPE DX, и MINDACT – генная экспрессия MAMMAPRINT). В обоих проектах в группах пациентов промежуточного риска, составивших около 75% популяции, не выявлено достоверной пользы от дополнительной к ЭТ ХТ. Некоторое (3–5%) улучшение выживаемости благодаря ХТ наблюдалось в испытании MINDACT у пременопузальных пациентов с высоким клиническим и молекулярным риском. Планирование лечение ER+ РМЖ, основанного на результатах исследований TAILOR и MINDACT, получило 1А-уровень доказательности [8, 9].
Общее голосование on-line на 12-й конференции EBCC (октябрь 2020 г.) показало, что 75% проголосовавших не поддерживали использование адъювантной ХТ при люминальном А-РМЖ без метастазов в региональных лимфоузлах (N0) и 33 против 67% голосовавших поддерживали дополнительное использование ХТ до адъювантной ЭТ при наличии регионарных метастазов (N+). В рекомендациях ESMO (2019) также предлагается назначение одной ЭТ при раннем люминальном А-РМЖ, за исключением случаев «со значительным распространением опухоли».
Таким образом, с помощью более точного иммуногистохимического определения фенотипа опухоли и при возможности дополнительного использования «генетических сигнатур» (Oncotype DX, Mammaprint, Predict) удается определить пациентов с люминальным А-РМЖ, нуждающихся только в адъювантной ЭТ без использования ХТ. Это важное достижение в деэскалации цитотоксического лечения.
Вместе с тем известно, что у значительного числа пациентов с люминальными (ER+) опухолями возникает рецидив заболевания через 5 и более лет после хирургического вмешательства. Когда и почему наступает резистентность к применяемой ЭТ, назначаемой в адъюванте на 5 и 10 лет? Клинически выявляемое наступление рецидива заболевания (обычно отдаленные метастазы) означает наступление резистентности к проводимой ЭТ. Скорее всего она возникает значительно раньше срока, клинически определяемого с помощью компьютерной (КТ), магнитно-резонансной томографии (МРТ), ультразвукового исследования (УЗИ) рецидива, и пациенты в течение нескольких месяцев и, во...












