Клиническая Нефрология №5-6 / 2015
Поражение сердца у больных атипичным гемолитико-уремическим синдромом
1 ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» МЗ РФ, клиника нефрологии, внутренних и профессиональных болезней им. Е.М. Тареева УКБ № 3, Институт профессионального образования, кафедра нефрологии и гемодиализа 2 ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» МЗ РФ, Институт профессионального образования, кафедра профилактической и неотложной кардиологии 3 ГБУЗ «Государственная клиническая больница им. А.К. Ерамишанцева» ДЗ Москвы, отделение нефрологии
В статье представлены 5 клинических наблюдений поражения сердца у пациентов с аГУС и обзор литературы, освещающий основные аспекты сердечно-сосудистой патологии у этого контингента больных. Проанализированы основные клинические проявления и особенности тромботической микроангиопатии миокарда. Предложено рассматривать ТМА как новую причину кардиоренального синдрома 5-го типа.
Введение
Атипичный гемолитико-уремический синдром (аГУС) – системное заболевание группы тромботических микроангиопатий (ТМА), обусловленное неконтролируемой активацией альтернативного пути комплемента вследствие генетического дефекта (мутации генов, кодирующих синтез белков – регуляторов системы комплемента) или реже – аутоиммунной патологии (выработка аутоантител к фактору Н – основному регуляторному протеину альтернативного пути) [1, 2]. Имеющиеся у пациентов с аГУС мутации в генах факторов Н (CFH), I (CFI), мембранного кофакторного протеина (MCP), тромбомодулина (THBD) обусловливают их количественный или чаще функциональный дефицит, что приводит к нарушению защиты эндотелия от атаки комплемента. Результатом этого становится усиленное образование на поверхности клеток мембрано-атакующего комплекса (МАК), вызывающего их повреждение с обнажением субэндотелиального матрикса, трансформацию атромботического фенотипа в протромботический, активацию тромбоцитов с последующим тромбообразованием в сосудах микроциркуляторного русла различных органов [3, 4]. Таким образом, аГУС представляет собой комплемент-опосредованную ТМА, характеризующуюся классической триадой симптомов – микроангиопатической гемолитической анемией (МАГА), тромбоцитопенией и острым почечным повреждением, поскольку именно почки служат основной (однако не единственной) мишенью микротромбообразования [5]. Атипичный ГУС имеет крайне высокий риск внезапной смерти и необратимых инвалидизирующих повреждений жизненно важных органов, включая почки, печень, сердце и головной мозг [6]. Хотя комплемент-опосредованная ТМА поражает главным образом сосуды почечной микроциркуляции, в последнее время все чаще отмечают экстраренальные проявления аГУС, которые развиваются не менее чем у 20% пациентов. Помимо упомянутых выше у больных аГУС описаны также поражения легких, желудочно-кишечного тракта, кожи, скелетных мышц, глаз. Такой широкий спектр экстраренальных проявлений, безусловно, свидетельствует об истинно системном характере комплемент-опосредованной ТМА. А тот факт, что эти проявления могут развиваться не только в момент острого эпизода ТМА, но и спустя несколько лет после его купирования, а также у пациентов, получающих диализную терапию (у которых, как полагали ранее, невозможно развитие новых эпизодов ТМА), лишь подтверждает представление о возможности хронического течения аГУС, обусловленного постоянно происходящей активацией комплемента, с вовлечением в патологический процесс новых бассейнов микроциркуляции [7, 8]. Полагают, что генерализация микроангиопатического процесса может быть связана с воздействием на организм все увеличивающегося числа различных неблагоприятных факторов, потенциально способных вызывать дополнительное повреждение эндотелия у лиц, имеющих генетический дефект регуляции системы комплемента (воспаление, лекарства, радиация, артериальная гипертензия и т.п.) [7].
Из всех экстраренальных проявлений аГУС наибольшее значение имеют поражение ЦНС и сердца, поскольку их патология может быть ассоциирована с неблагоприятным прогнозом. Точная распространенность поражения сердца и степень его влияния на общий прогноз при аГУС не известны, что обусловлено отсутствием характерной клинической картины и, следовательно, общепринятых критериев обследования данных пациентов. Между тем есть основания полагать, что при аГУС, как и при любой ТМА, возможно поражение сердца различной степени тяжести, вплоть до развития некоронарогенного инфаркта миокарда [9–11], обусловленного тромбозами мелких интрамиокардиальных сосудов. В настоящей статье мы хотели бы продемонстрировать различные варианты нарушения сердечной функции у пациентов с аГУС.
Пациенты и методы
Нами были проанализированы клинические проявления 17 больных аГУС, наблюдавшихся в клинике нефрологии им. Е.М. Тареева Первого МГМУ им. И.М. Сеченова и нефрологическом отделении ГКБ им. А.К. Ерамишанцева Москвы в 2010–2013 гг. У 5 (29,4%) из них выявлены различные документально подтвержденные признаки поражения сердца. Приводим наши наблюдения.
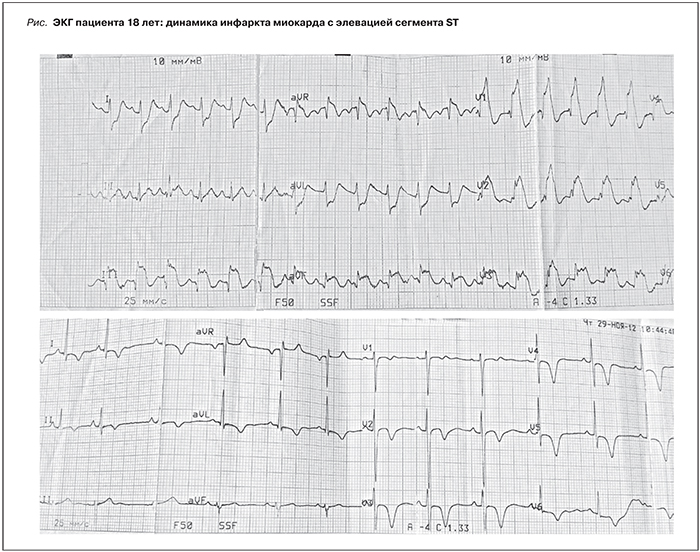
Пациент 1 18 лет. Летом 2012 г. после введения противостолбнячной сыворотки развился нефротический синдром (НС). Проводимая в течение 3 месяцев иммуносупрессивная и диуретическая терапия оказалась неэффективной, отеки быстро наросли до степени анасарки, в связи с чем в октябре 2012 г. был госпитализирован в нефрологическую клинику Первого МГМУ им. И.М. Сеченова. При обследовании картина развернутого НС (суточная протеинурия (СПУ) 8 г/сут, альбумин крови 22 г/л), олигурия, анасарка, креатинин крови 1,2 мг/дл, СКФ 61 мл/мин. Обращала на себя внимание анемия (гемоглобин 119 г/л), повышение уровня ЛДГ (990 ЕД/л). В связи с резистентностью отеков к массивной диуретической терапии проведено 13 сеансов ультрафильтрации, в результате чего отеки уменьшились, вес пациента снизился на 15 кг. Однако выраженность ...












