Акушерство и Гинекология №5 / 2021
Предимплантационное генетическое тестирование с применением метода гаплотипирования с помощью однонуклеотидных полиморфизмов
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Министерства здравоохранения Российской Федерации, Москва, Россия
Цель. Разработка и применение метода гаплотипирования с помощью однонуклеотидных полиморфизмов (SNP) для предимплантационного генетического тестирования моногенных заболеваний (ПГТ-М) с использованием чипов Affymetrix Inc., США.
Материалы и методы. Были обследованы 23 семьи с моногенной патологией. Использовали комплексный подход с одновременным применением ПГТ-М (фрагментный анализ STR-маркеров, SNP-гаплотипирование, секвенирование по Сэнгеру, полимеразная цепная реакция в реальном времени) и ПГТ анеуплоидий (ПГТ-А) (NGS и aCGH).
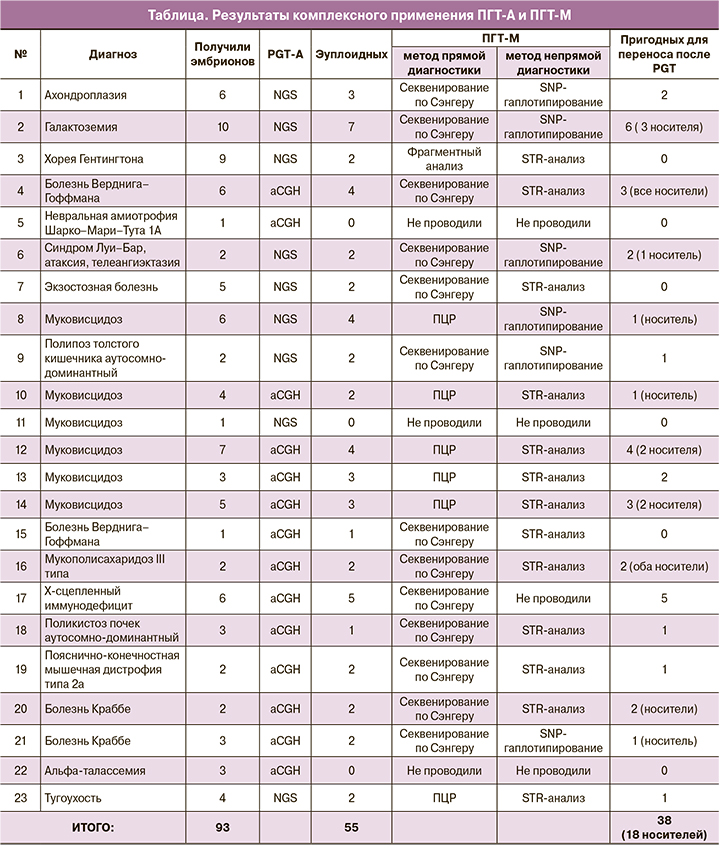
Результаты. Из 93 направленных на тестирование эмбрионов эуплоидными оказались 55. В трех семьях ПГТ-М не проводили из-за полного отсутствия эуплоидных эмбрионов после ПГТ-А.
В остальных 20 наблюдениях перенос в полость матки оказался возможен для 38 эмбрионов (20 – без мутаций и 18 – гетерозиготные носители). Установлено, что интерпретация результатов SNP-гаплотипирования более проста и надежна по сравнению с STR-анализом. Данная методика не требует индивидуальной разработки для каждого случая и является универсальной. Подробно описаны результаты применения SNP-гаплотипирования для двух случаев: ПГТ-М ахондроплазии (аутосомно-доминантный тип наследования) и галактоземии (рецессивный тип наследования).
Заключение. Универсальность и надежность разработанного подхода значительно ускоряют получение результатов, облегчают их интерпретацию и снижают вероятность возможных ошибок. Также проведению ПГТ-М должно предшествовать ПГТ-А для профилактики хромосомной патологии.
Предимплантационная генетическая диагностика (ПГД) – это диагностика генетических нарушений эмбриона в рамках программы вспомогательных репродуктивных технологий (ВРТ) до его переноса в полость матки пациентки [1]. Обследование проводится с целью профилактики рождения больных детей у семейных пар с известными генетическими нарушениями, которые могут быть унаследованы их детьми. В настоящее время используется термин ПГТ-М – предимплантационное генетическое тестирование моногенных заболеваний [2]. Для ПГТ-М используются различные методики. Их можно разделить на два класса – прямые и непрямые методы исследования [3]. Прямые методы исследования способны обнаруживать непосредственное генетическое нарушение (генная или хромосомная мутация, являющаяся причиной развития заболевания). Однако использование только прямых методов исследования может быть недостаточным из-за эффекта «выпадения» аллелей (allele drop-out) [1].
Непрямые методы исследования не способны обнаруживать непосредственное генетическое нарушение, однако с их помощью возможно отследить наследование соответствующих участков хромосом от родителей. Классическим методом непрямой ПГТ-М является фрагментный анализ STR-маркеров. Он основан на анализе коротких тандемных повторов (STR, short tandem repeats) [4]. Данный подход также не лишен недостатков. Во-первых, для успешного тестирования необходимы разработка соответствующих методик и время на их валидацию. Во-вторых, как уже отмечалось выше, для каждого тестирования необходимо сразу несколько таких методик, так как, кроме проблемы выпадения аллеля, возможно, что часть маркеров будет неинформативной из-за совпадения у отца и матери.
В 2010 г. для проведения ПГТ-М был предложен универсальный метод, основанный на картировании однонуклеотидных полиморфизмов в родительских хромосомах, который получил название «кариомэппинг» [5]. За счет своих технологических особенностей данный метод позволяет проводить ПГТ-М очень быстро, а интерпретация результатов с его помощью относительно проста. Он может быть использован для тестирования любых семейных моногенных заболеваний без необходимости разработки и валидации пациент-специфического теста.
Метод представляет собой полногеномный сцепленный анализ, в котором несколько сотен тысяч единичных нуклеотидных последовательностей (SNP), разбросанных по всему геному, генотипированы у обоих родителей и эмбриона. Каждый регион хромосомы имеет уникальный SNP-отпечаток, позволяющий отслеживать наследование сегментов хромосом (или генов, которые они содержат) от одного поколения к другому. Путем сравнения результатов SNP члена семьи с установленным генетическим заболеванием с родительскими (т.е. другого родственника, несущего такую же мутацию) возможна идентификация мутантного гена за счет комбинации ассоциированных SNP-аллелей. В результате перенос эмбриона, несущего патологическую хромосому (определенную по SNP-локусам), проводиться не будет.
Кариомэппинг является дорогостоящим методом и описан лишь для одной платформы на базе биологических чипов фирмы Illumina, что ограничивает его повсеместное применение. Однако в настоящее время существует высокая клиническая потребность в подобных методах, не привязанных к ограниченному числу технологических платформ. Это привело к разработке ряда альтернативных методов на том же принципе [6, 7].
Целью данной работы были разработка и применение метода гаплотипирования с помощью SNP для ПГТ-М с использованием чипов Affymetrix Inc., США.
Материалы и методы
В лаборатории молекулярно-генетических методов Центра с помощью ПГТ были обследованы 23 семьи с моногенной патологией (у обратившихся пациентов, их детей или родственников). Характер патологии представлен в таблице 1. В связи с малым количеством поступившего для анализа материала (трофэктодермы) исследование начинали с применения методов полногеномной амплификации ДНК. Выбор метода зависел от применяемых в дальнейшем способов тестирования. При применении SNP-гаплотипирования использовали MDA (Qiagen, USA), в остальных случаях WGA-PCR (Picoplex, USA).
Тестирование представляло собой комплексный подход с одновременным применением ПГТ-М и ПГТ анеуплоидий (ПГТ-А). Для проведения ПГТ-М были использованы следующие методы: фрагментный анализ STR-маркеров, SNP-гаплотипирование, секвенирование по Сэнгеру, полимеразная цепная реакция (ПЦР) в реальном времени для анализа наиболее частых мутаций (например, F508del при муковисцидозе, GJB2: 35delG при врожденной нейросенсорной тугоухости). ПГТ-А осуществляли с помощью высокопроизводительного секвенирования (NGS) (ReproSeq™ PGS Kit Thermo Fisher Scientific, USA) и сравнительной геномной гибридизации на чипах (aCGH) (GenetiSure Agilent, USA).
Подход к SNP-гаплотипированию был разработан в рамках настоящего исследования. Пробоподготовка предоставленных образцов включала рестрикцию, лигировани...












