Урология №6 / 2017
Применение 3D-мягких печатных моделей почки для лечения больных локализованным раком почки (пилотное исследование)
Первый МГМУ им. И. М. Сеченова (Сеченовский Университет), НИИ уронефрологии и репродуктивного здоровья человека, Москва, Россия
Цель: оценить возможность применения 3D-печати в урологии для лечения пациентов
локализованным раком почки.
Материалы и методы. В исследование вошли 5 пациентов с локализованным раком почки, находившихся на лечении в клинике урологии Первого МГМУ им. И. М. Сеченова с января 2016 по апрель 2017 г. Наряду со стандартным обследованием пациентам была выполнена мультиспиральная компьютерная томография (МСКТ), на основании данных которой с помощью 3D-моделирования и 3D-печати были изготовлены индивидуальные 3D-печатные модели почки с опухолью. Для оценки эффективности использования 3D-печатных моделей было проведено двухэтапное предоперационное планирование с анкетированием 5 хирургов (анкета состояла из 4 вопросов и вариантов ответов). На первом этапе планирование операций осуществлялось по данным МСКТ больных. На втором к имеющимся данным были предоставлены индивидуальные 3D-модели почки с опухолью. В каждом наблюдении хирургами был проведен предоперационный тренинг на мягких 3D-печатных моделях почки с опухолью. После предоперационного тренинга больным были выполнены лапароскопические резекции почки с опухолью.
Результаты. По результатам анкетирования, каждый из участвовавших хирургов хотя бы
1 раз изменил свою хирургическую тактику лечения на основании данных, полученных с помощью 3D-печатных моделей почки с опухолью.
Выполнение предоперационного тренинга с использованием 3D-печатных моделей почки оказалось эффективным.
Всем пациентам были проведены эндоскопические пособия лапароскопическим доступом одним хирургом с большим опытом выполнения данного вида оперативных вмешательств. Среднее время оперативных пособий составило 187 мин. Все пособия выполнены с перекрытием основной почечной артерии. Среднее время тепловой ишемии составило 19,5 мин., средний объем кровопотери – 170 мл. Конверсий в открытые пособия и органоуносящих вмешательств не было. Послеоперационных осложнений и летальных исходов не наблюдалось. Все хирургические края были отрицательными. В четырех наблюдениях морфологически верифицирован почечно-клеточный рак, у одной больной верифицирована онкоцитома.
Заключение. В исследовании продемонстрирована перспективность использования 3D-печати для дооперационного планирования и исполнения операций, позволяющего создать высокоточную трехмерную мягкую физическую модель с локализованным раком почки конкретно каждого пациента.
Введение. Во всем мире в структуре всех злокачественных онкологических заболеваний с частотой 2,4% почечно-клеточный рак (ПКР) занимает 12-е место. Ежегодно данная патология приводит к смерти около 140 тыс. пациентов [1]. Только в Российской Федерации с 2010 по 2014 г. зарегистрировано около 100 тыс. новых случаев. Ежегодный прирост заболеваемости составляет около 3–4% [2].
В связи с развитием и совершенствованием методов лучевой диагностики в последнее время ПКР все чаще выявляется на ранних стадиях, как правило Т1 [3–5]. В 50% случаев это является «случайной» находкой при УЗИ или мультиспиральной компьютерной томографии (МСКТ), магнитно-резонансной томографии (МРТ) [6]. Особенность опухолевого процесса в почке при стадии Т1–Т2 состоит в стертой клинической картине, зачастую имеет место бессимптомное течение [7].
На протяжении десятилетий «золотым» стандартом в лечении рака почки стадии Т1–Т2 считалась радикальная нефрэктомия. Однако в ходе проведенных в последнее время исследований установлено, что продолжительность жизни больных, подвергшихся органосохраняющему оперативному вмешательству при малых размерах опухоли (до 4 см), гораздо выше за счет снижения риска развития сердечно-сосудистых заболеваний [8, 9]. Понимание важности сохранения большего объема функционирующей почечной ткани, а также последующее появление минимально инвазивных методик лечения существенно сократили показания к полному удалению почки [10].
С момента первого сообщения Clayman в 1991 г. о применении лапароскопического доступа для лечения рака почки его стали широко использовать при хирургическом лечении данной категории больных [11]. В настоящее время все чаще проводятся высокотехнологичные оперативные пособия в объеме лапароскопических и робот-ассистированных операций.
Выбор в пользу минимально инвазивных лапароскопических и робот-ассистированных подходов при решении вопроса об органосберегающих операциях на почке обеспечивает скорейшее выздоровление пациентов и сокращение сроков госпитализации, при этом позволяя соблюдать принципы онкологической абластичности и эффективности [12].
В настоящее время помимо стандартных УЗИ, МСКТ и МРТ как методов предоперационного обследования широкое распространение получает 3D-моделирование – техника, позволяющая получать объемное, информативное изображение патологического процесса [13]. Данный метод существенно расширил границы применения лучевых методов исследования, хотя и он – всего лишь графическое представление той или иной области.
 Эволюция так называемых аддитивных методов производства способствовала внедрению в медицину 3D-печати – современной технологии, позволяющей на дооперационном этапе получать объемную модель органа.
Эволюция так называемых аддитивных методов производства способствовала внедрению в медицину 3D-печати – современной технологии, позволяющей на дооперационном этапе получать объемную модель органа.
Как известно, любой опухолевый процесс уникален. Местоположение, глубина и ориентация опухоли по отношению к чашечно-лоханочной системе (ЧЛС), артериям и венам широко вариабельны, поэтому неоспоримое достоинство 3D-печати – это возможность создания строго индивидуальных для каждого пациента 3D-моделей, являющихся точной копией срезов его двухмерного снимка, полученного с помощью лучевых методов исследования (МСКТ или МРТ).
Особенно интересен этот метод при опухолях почки стадии T1–T2, так как, согласно рекомендациям Американской и Европейской ассоциаций урологов, операцией выбора в подобных случаях является резекция почки [14, 15].
На сегодняшний день в мире исследований, посвященных применению 3D-печати, немного, а в России подобных исследований не проводилось.
Цель исследования: оценить возможность применения 3D-печати в урологии для лечения пациентов с локализованным раком почки.
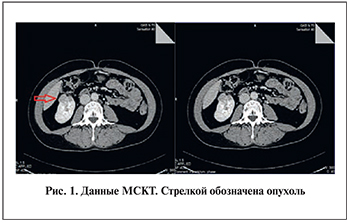
Материалы и методы. В исследование вошли 5 пациентов, у которых по результатам предоперационных лучевых исследований (УЗИ) были диагностированы новообразования почки. Эти больные находились на лечении в клинике урологии Первого МГМУ им. И. М. Сеченова с января 2016 по апрель 2017 г. На дооперационном этапе каждому пациенту была проведена МСКТ с контрастным усилением на аппарате Toshiba Aquilion One 640 (Япония; рис. 1). Положение пациента – лежа на спине. Параметры съемки: режим исследования спиральный, толщина среза – 0,5 мм, напряжение – 120 кВ, сила тока – 80 мА, скорость вращения трубки – 0,5 с, зона исследования: от купола диафрагмы до лобкового сочленения; внутривенное контрастирование: контрастный препарат «Ультравист-370» – 80–90 мл, скорость введения – 3,5–4 мл в 1 с. Получена информация обо всех четырех фазах исследования почек.
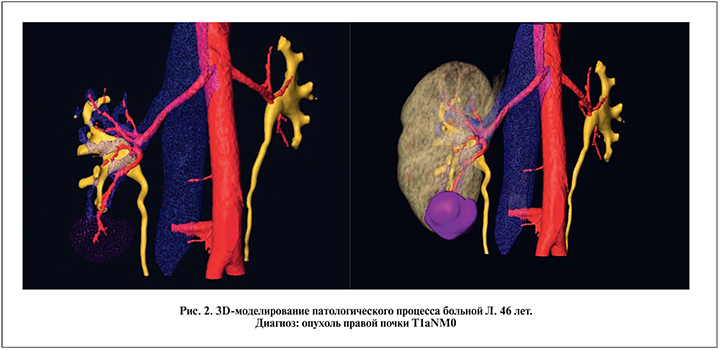
Следующий этап – получение виртуальных 3D-моделей (рис. 2). Для получения трехмерных объектов мы использовали программу Amira компании VSG версии 5.4.5 (лицензия ASTND.44644), которая обрабатывает данные МСКТ, полученные в формате DICOM (...












