Фарматека №9 (362) / 2018
Профилактика моторно-эвакуаторных нарушений в послеоперационном периоде после ликвидации острой неопухолевой тонкокишечной непроходимости
Московский государственный медико-стоматологический университет им. А.И. Евдокимова, Москва, Россия
Обоснование. Послеоперационные моторно-эвакуаторные нарушения играют важную роль и занимают значительную долю в структуре осложнений после абдоминальных оперативных вмешательств. Лечение острой спаечной кишечной непроходимости помимо непосредственного восстановления пассажа химуса требует проведения парциального или тотального адгезиолизиса, что может стать плацдармом для нарушений моторики вследствие отека кишечной стенки, травмы брюшины, эффекта денудации и для нового формирования спаечных сращений. Цель: оценка эффективности резонансной электростимуляции в комплексной коррекции моторно-эвакуаторных нарушений у пациентов в послеоперационном периоде после устранения острой неопухолевой тонкокишечной непроходимости. Методы. Анализу подвергнуты 65 историй болезней пациентов, находившихся на стационарном лечении за 2015–2018 гг. Средний возраст составил 53,4±3,7 года, гендерное распределение с преобладанием мужского пола – 1,5:1. Группы были разделены на основную (n=33, стандартное ведение послеоперационного периода с дополнительным применением резонансной электростимуляции) и группу сравнения (n=32; стандартное послеоперационное ведение больных). Группы были полностью соизмеримыми по полу, возрасту, объему операции, тяжести состояния (р≥0,05). Больные оперированы по поводу неопухолевой тонкокишечной непроходимости лапаротомным доступом. Результаты. На фоне резонансной стимуляции в основной группе отмечен более быстрый эффект восстановления моторно-эвакуаторной функции кишечника. Полное восстановление функции пищеварительного тракта в основной группе отмечено к 5-м суткам лечения у 33 (100%) пациентов, что достоверно отличалось от тождественных параметров группы сравнения (n=26; 81,25%; p≤0,05). Осложнения по шкале D. Dindo et al.: в группе сравнения 7 (21,9%; р≤0,05) случаев пареза кишечника, в основной данное осложнение не зарегистрировано. Длительность послеоперационного стационарного лечения в группе сравнения была достоверно выше (9,3±1,3 суток), чем в основной группе (6,2±0,8 суток; p≤0,05). Заключение. Применение резонансной электростимуляции в комплексном ведении послеоперационного периода способствует более быстрой нормализации перистальтики, восстановлению пассажа кишечного содержимого по пищеварительному тракту, скорейшей нормализации внутрибрюшной гипертензии и профилактике полиорганной недостаточности.
Актуальность
Начало XXI в. ознаменовалось содружественным ростом как числа оперативных вмешательств в экстренной и плановой абдоминальной хирургии, так и числом пациентов со спаечным процессом брюшины. Последний аспект по сути служит «миной замедленного действия» в плане развития острой спаечной кишечной непроходимости, что встречается в 30–67% случаев наличия спаечного процесса [1, 2]. Несмотря на бурное развитие анестезиолого-реаниматологической службы, внедрение программ ускоренной реабилитации, применение всего спектра малоинвазивных технологий, на сегодняшний день частота регистрации острого спаечного илеуса не имеет тенденции к снижению, а послеоперационная летальность может достигать внушительных цифр (8,1–22%) [3].
Возникновение внутрибрюшных висцеро-висцеральных и париетальных сращений возможно после любого трансперитонеального вмешательства: в пределах 67–93% после операций обшехирургического профиля и до 95–97% после гинекологических вмешательств, особенно при применении лапаротомного доступа [2, 4–6]. Важен рост материальных затрат на оказание специализированной помощи пациентов со спаечной болезнью брюшины, что сопряжено с необходимостью повторных, а порой многократных операций [7]. Имеются данные о ежегодно госпитализируемых 117 человек на 100 тыс. населения с общими затратами на их лечение в 1,3 млн долл. лишь только в США [4].
К сожалению, выполнение оперативного пособия на фоне спаечной кишечной непроходимости способствует осложнению раннего послеоперационного периода явлениями моторно-эвакуаторных нарушений в виде паралитического илеуса или ранней спаечной кишечной непроходимости. Риск вероятности рецидива спаечной болезни при проведении оперативного вмешательства возрастает при отеке кишечной стенки, явлениях «денудации» брюшины, необходимости объемного адгезиолизиса и возможной десерозации кишечной стенки, диапедеза из области спаечных сращений и создания плацдарма для неоадгезиоформации. Проведенные исследования убедительно доказали прямую связь между регистрацией пареза и ростом затрат на лечение подобных больных, что в числовом эквиваленте выражается в увеличении затрат на 8316 долл. на пациента при выполнении колоректальных хирургических операций [8]. Развитие динамической послеоперационной кишечной непроходимости приводит к пролонгации госпитального (порой и реанимационного) этапа лечения в 1,5–2 раза [9]. Суммарные ежегодные затраты на лечение подобных пациентов по оценочным данным превышают 750 тыс. долл. [9, 10].
Частота возникновения послеоперационных моторно-эвакуаторных нарушений пищеварительного зависит от многих факторов, в т.ч. от типа операции: операции с лапаротомным доступом и манипуляциями с петлями кишечника имеют большую вероятность развития пареза, чем операции с минимальной агрессией в брюшной полости (например, холецистэктомия) [11]. По мнению A. Artinyan et al. [8], независимыми факторами риска пареза следует считать объем интраоперационной кровопотери, суммарную дозу опиоидных анальгетиков, а также ожирение [12]. Риск развития динамических нарушений пищеварительного тракта повышается при наличии синдрома системной воспалительной реакции (p<0,01), коморбидности патологии (p=0,02), высокой степени анестезиологического риска (p=0,01), а также после операции с использованием открытого доступа [11]. Важно отметить, что пациенты с явлениями острой кишечной непроходимости имеют статически более высокий риск развития динамической послеоперационной кишечной непроходимости [11, 13].
Приведенные выше данные диктуют необходимость не только лечения непосредственно спаечной болезни, осложненной острой спаечной тонкокишечной непроходимостью, но и профилактики и терапии моторно-эвакуаторных нарушений пищеварительного тракта в послеоперационном периоде.
Целью настоящего исследования стала оценка эффективности резонансной электростимуляции перистальтической активности пищеварительного тракта в комплексной коррекции моторно-эвакуаторных нарушений у пациентов в послеоперационном периоде после устранения острой неопухолевой тонкокишечной непроходимости.
Методы
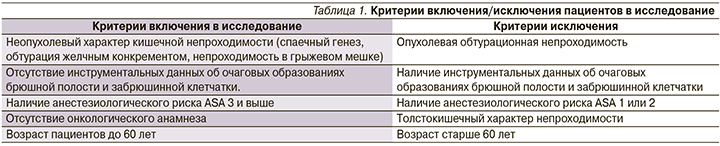
В ходе работы был подвергнут анализу исход лечения 65 пациентов за 2015–2018 гг., находившихся на стационарном лечении в хирургических клиниках кафедры хирургических болезней и клинической ангиологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова. Все пациенты, включенные в исследование, удовлетворяли критериям включения и исключения (табл. 1). Критерием невключения в исследование считался письменный отказ пациента. Опухолевый характер кишечной непроходимости был не случайно выбран противопоказанием к включению в исследование, т.к. выполняемая операция (с учетом онкологических принципов) требует проведения должного объема лимфодиссекции, а также не всегда позволяет завершить операцию без колостомии. Последние аспекты служат отягощающим неспецифическим фактором в развитии ...












