Фарматека №s1-16 / 2016
Радикальная позадилонная и робот-ассистированная простатэктомия у больных локализованным раком предстательной железы: сравнительный анализ онкологических и функциональных результатов
Кафедра урологии ГБОУ ВПО МГМСУ им А.И. Евдокимова Минздрава России, Москва
В исследовании, включавшем 583 пациента с локализованным раком предстательной железы (РПЖ), проведен сравнительный анализ эффективности робот-ассистированной (РА) радикальной простатэктомии (РПЭ) и радикальной позадилонной РПЭ (РПЛПЭ) c позиции достижения оптимального онкологического и функционального результатов. Первую группу составили 512 пациентов, которым была выполнена РА РПЭ. Вторую группу составил 71 пациент, перенесший РПЛПЭ. Медиана наблюдения составила в группе РА РПЭ 38,9 месяца (max 63,9), в группе РПП 22,6 месяца (max 46). Группы были сравнимы между собой по возрасту, сопутствующей патологии и онкологическим характеристикам. Подчеркивается, что РПЭ является золотым стандартом хирургического лечения локализованного РПЖ. По данным анализа современной литературы и нашим собственным данным следует констатировать, что независимо от техники выполнения – позадилонной или РА, РПЭ обеспечивает высокий онкологический результат и удовлетворительные показатели безрецидивной и раково-специфической выживаемости. С другой стороны, использование РА выполнения РПЭ оказалось существенно более эффективной с точки зрения вероятности послеоперационного удержания мочи и восстановления эректильной функции в течение 12 месяцев после операции. Существенные различия наблюдаются не только в общей доле пациентов, у которых достигнут хороший функциональный результат, но и в темпах восстановления функции.
Введение
На сегодняшний день радикальная простатэктомия (РПЭ) является основным методом лечения локализованного рака предстательной железы (РПЖ). Смертность от этого заболевания в течение 15 лет с момента выполнения радикальной простатэктомии составляет 7–20%. При этом выживаемость без биохимического рецидива заболевания за аналогичный период наблюдений может достигать 75% [1, 2]. Необходимо отметить, что эти данные были получены в результате наблюдения за пациентами, перенесшими открытую радикальную позадилонную простатэктомию (РПЛПЭ), которая была выполнена в ряде крупных европейских клиник. Однако сегодня в США и странах Западной Европы большинство таких операций выполняется с помощью роботической системы DaVinci [3].
Согласно положению ВОЗ, полное здоровье – это не только избавление от заболевания, но и психическая, эмоциональная, физическая и социальная реабилитация после перенесенного лечения. Иными словами – это радикальное избавление от заболевания и высокое качество жизни. Независимо от техники ее выполнения РПЭ преследует цель избавления пациента от злокачественного процесса в ПЖ и является, по сути, онкологической операций. Именно поэтому анализ онкологических результатов операции представляет наибольший интерес для оценки эффективности хирургических методик. Существует несколько формальных критериев оценки онкологической эффективности – фиксация частоты позитивного хирургического края (ПХК), биохимический рецидив, общая и раково-специфическая выживаемость [5].
При оценке качества жизни после РПЭ учитываются такие критерии, как общая оценка пациентом результатов лечения, сексуальная реабилитация, способность удерживать мочу и т.д. Недержание мочи – одно из самых социально дезадаптирующих и поэтому крайне негативных последствий РПЭ. Проводя обязательную беседу с пациентом и его родственниками перед операцией, мы в клинике традиционно обсуждаем возможные осложнения, последствия и несостоятельность хирургического лечения. Исходя из опыта подобных бесед, не бывает пациентов, спокойно относящихся к перспективе возможного недержания мочи после операции. Даже ухудшение или утрата сексуальной функции не вызывает столько беспокойства, как недержание мочи [6].

Мы провели сравнительный анализ эффективности робот-ассистирован-ной (РА) РПЭ и РПЛПЭ c позиции достижения оптимального онкологического и функционального результатов.
Материал и методы
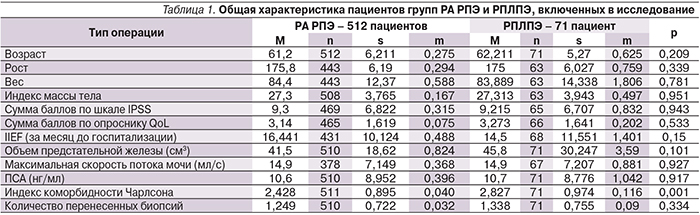
В настоящее ретроспективное исследование вошли две группы пациентов с верифицированным локализованным РПЖ, перенесших хирургическое лечение в период с декабря 2008 по декабрь 2013 г. в клинике урологии МГМСУ им. А.И. Евдокимова. Первую группу составили 512 пациентов, которым была выполнена РА РПЭ. Вторую группу составил 71 пациент, перенесший РПЛПЭ. Медиана наблюдения составила в группе РА РПЭ 38,9 (max 63,9), в группе РПП – 22,6 месяца (max 46). Группы были сравнимыми по возрасту, сопутствующей патологии и онкологическим характеристикам. Подробная демографическая характеристика пациентов приводится в табл. 1.
На рис. 1 представлено распределение пациентов согласно исходному баллу злокачественности по системе градации Глисона. В обеих группах подавляющее большинство пациентов до операции имели балл Глисона 3+3=6 и лишь у 6% пациентов в каждой группе суммарный балл превышал 8 при различном сочетании первичного и вторичного баллов.
Основным онкологическим показателем, отражающим распространенность опухолевого поражения, является стадия заболевания по системе TNM. На рис. 2 приведено распределение больных согласно дооперационно выставленным стадиям заболевания в процентах в обеих исследуемых группах. Не отмечено статистически достоверной разницы этого показателя между группами (р=0,013).
Желая структурировать прогноз и жалобы пациентов, мы выделили два понятия – немедленное удержание мочи (достижение полного контроля над мочеиспусканием в течение первых 3 суток после удаления уретрального катетера) и собственно удержание мочи – функцию, восстановление которой может быть пролонгировано во времени начиная с 4-го дня после удаление катетера и далее. Абсолютно идеальный результат – полное удержание сразу после удаления уретрального катетера. Под полным удержанием мочи мы понимаем состояние, которое, согласно критериям International Continence Society, определяется как отсутствие подтекания мочи в покое или при физической нагрузке с возможным использованием одной прокладки в сутки в качестве страховочной.
При наличии заинтересованности пациента в сохранении эректильной функции, сумме баллов по шкале Глисона не более 7, признаках локализованного поражения простаты по данным предварительного обследования, ПСА не более 10 нг/мл, мы обеспечили сохранение сосудисто-нервных пучков (СНП). Сохранение СНП оценивалось нами по описанию препаратов патоморфологом в зависимости от наличия структур СНП в удаленном препарате. В зависи...












