Кардиология №3 / 2014
Ренин-ангиотензин-альдостероновая система при гипертрофической кардиомиопатии
ГБОУ ВПО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздрава РФ, 119991 Москва, ул. Трубецкая, д.8, стр. 2
С целью изучения роли ренин-ангиотензин-альдостероновой системы (РААС) в формировании клинических вариантов течения гипертрофической кардиомиопатии (ГКМП) проведено исследование, включившее когорту больных ГКМП (n=58) и сопоставимую по полу и возрасту контрольную группу. Всем участникам исследования определяли полиморфизмы генов AGTR1 A1166C rs5186;
CYP11B2-344 T/C rs1799998; СМА1 A(-1903)G rs1800875; AGТ M235T rs699 и маркеры: ангиотензин II (АТII), ангиотензинпревращающий фермент (АПФ). Выявлено значительное снижение уровня АТII у больных ГКМП по сравнению с контрольной группой. Уровень маркера АТII коррелировал с толщиной задней стенки левого желудочка. Обнаружена связь показателей гипертрофии миокарда
с неблагоприятными аллельными вариантами генов ангиотензиногена и химазы. Генотип AG изучаемого полиморфизма гена химазы ассоциировался с желудочковой экстрасистолией высоких градаций и стенокардией II—III функционального класса. Полученные данные свидетельствуют не только о значительной роли РААС в формировании фенотипических проявлений, но и позволяют разработать новые подходы к прогнозированию неблагоприятных клинических исходов.
Гипертрофическая кардиомиопатия (ГКМП) — генетически обусловленное заболевание, которое может иметь как благоприятное, так и тяжелое течение, характеризующееся развитием фатальных осложнений, приводящих к инвалидизации и смерти людей молодого возраста [1]. Эпидемиология ГКМП в России практически не изучена, что обусловлено, с одной стороны, отсутствием крупных популяционных исследований, а с другой, — часто бессимптомным течением, при котором единственным проявлением заболевания может быть внезапная сердечная смерть (ВСС). По расчетным данным, составленным с учетом коэффициентов в ходе эпидемиологических исследований стран Европы и США, возможная частота ВСС в России составляет 141—460 тыс. в год. [2]
Ранняя оценка прогноза течения заболевания, своевременное начало и правильный выбор тактики лечения существенно снижают уровень сердечно-сосудистой инвалидизации и смертности у этих больных. Поэтому актуальной проблемой остается поиск методов ранней диагностики ГКМП и способов оценки риска развития неблагоприятных клинических исходов.
В настоящее время продолжаются активный поиск и исследование многочисленных потенциальных генов-модификаторов, способных влиять на фенотипические проявления различных сердечно-сосудистых заболеваний (ССЗ), в частности ГКМП.
Доказано, что ренин-ангиотензин-альдостероновая система (РААС) участвует в развитии ремоделирования сердечно-сосудистой системы при ГКМП (развитие гипертрофии миокарда, пролиферация фибробластов, нарушение фибринолиза, стимуляция синтеза коллагена, накопление внеклеточного матрикса), что может иметь большое значение для формирования вариантов клинического течения [3—5].
Актуальной представляется оценка маркеров нейрогуморальных систем у больных ГКМП с различными вариантами течения, так как эта область остается мало изученной.
Целью нашего исследования послужило изучение роли полиморфизмов генов, кодирующих компоненты РААС (AGT, AGTR1, CYP11B2, CMA1) и маркеров, характеризующих эту систему (АСЕ и АТII), у больных ГКМП с различными вариантами клинического течения.
Материал и методы
 Обследованы 58 больных ГКМП (24 мужчины и 34 женщины), наблюдающихся в клинике госпитальной терапии №1 Первого МГМУ им. И.М. Сеченова, не связанных узами родства, средний возраст которых составил 48,4±13,6 года. В контрольную группу вошли 54 здоровых добровольца (22 мужчины, 32 женщины), средний возраст которых составил 49,3±13,5 года и не отличался от такового у пациентов исследуемой группы (р=0,95).
Обследованы 58 больных ГКМП (24 мужчины и 34 женщины), наблюдающихся в клинике госпитальной терапии №1 Первого МГМУ им. И.М. Сеченова, не связанных узами родства, средний возраст которых составил 48,4±13,6 года. В контрольную группу вошли 54 здоровых добровольца (22 мужчины, 32 женщины), средний возраст которых составил 49,3±13,5 года и не отличался от такового у пациентов исследуемой группы (р=0,95).
Диагноз ГКМП устанавливали согласно рекомендациям по диагностике и лечению больных ГКМП. В отсутствие фенотипических проявлений проводили молекулярно-генетическое исследование.
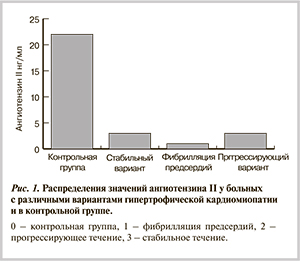
Больные были разделены на группы по вариантам клинического течения: стабильное течение (n=21, 36,2%); вариант с фибрилляцией предсердий — ФП (n=10, 17,2%); прогрессирующее течение ГКМП (n=27, 46,6%). Все пациенты проходили стандартное клиническое обследование.
Эхокардиографию (ЭхоКГ) проводили на аппарате Vivid7 Dimension/Vivid 7 PRO версия 6.0.х (Германия) по методике двухмерной ЭхоКГ с использованием М- и В-режимов, а также с использованием импульсно-волнового и непрерывно-волнового допплеровских режимов. Оценивали размеры камер сердца, основные показатели гипертрофии миокарда, в том числе толщину межжелудочковой перегородки (ТМЖП) и задней стенки левого желудочка (ТЗСЛЖ). Определяли также показатели диастолической дисфункции, нарушения глобальной и локальной сократимости миокарда. На основании полученных данных, согласно стандартизованным математическим формулам, производили вычисление следующих параметров: массы миокарда ЛЖ (ММЛЖ), индекса массы миокарда ЛЖ (ИММЛЖ), отношения между наполнением ЛЖ в диастолу – пик Е и систолу предсердий – пик А (Е/А), индекса объем-масса (ИОМ), предсердно-желудочкового отношения (ПЖО) [6].
Анализ полиморфизмов генов-модификаторов. У всех больных определяли полиморфизмы генов-модификаторов, характ...












