Фарматека №2 (275) / 2014
Результаты исследования эффективности пробиотиков и коррекции моторики кишечника при СРК у детей
ГБОУ ВПО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России, Санкт-Петербург
Целью настоящего исследования стало проведение сравнительной оценки эффективности терапии пробиотиками или препаратами, координирующими моторику кишечника (тримебутином) у пациентов с синдромом раздраженного кишечника (СРК). Под наблюдением находился 121 пациент в возрасте от 5 до 17 лет с нарушениями, соответствующими клиническим критериям СРК. В зависимости от проводимой терапии больные были разделены на семь групп. Наибольший эффект по купированию симптомов СРК был достигнут в группе комбинированной терапии (тримебутин + пробиотик). Среди пробиотиков при монотерапии разными препаратами наилучший результат получен от курса лечения Энтеролом. Результаты исселования подтверждают целесообразность воздействия на ключевые точки «порочного круга», свойственного СРК.
Патогенез синдрома раздраженного кишечника (СРК) остается предметом дискуссий, поскольку в его формировании принимают участие разные механизмы. В 1973 г. Ritcher первым описал висцеральную гиперчувствительность пациентов с СРК, которая является ведущим звеном в патогенезе клинических проявлений заболевания [1]. Последующие исследования показали, что при СРК порог болевой чувствительности снижен на 50–70 % по сравнению с нормой. В соответствии с концепцией гиперчувствительности пациенты с СРК сильнее, чем группа контроля, реагируют на сократительную активность кишки [2]. В исследованиях W.E. Whitehead с помощью баллонного теста был подтвержден феномен висцеральной гиперчувствительности, которая не распространяется на восприятие соматической боли [3]. В интересном эксперименте с погружением кисти руки в холодную воду t = 4 ºС было показано, что и общая чувствительность при функциональных расстройствах кишечника повышена у пациентов с СРК: они быстрее, чем контрольная группа, испытывали неприятные ощущения и раньше заканчивали эксперимент. Однако нарушение толерантности, продемонстрированное в тесте с холодной водой, не имело связи с возрастом, типом функциональных расстройств и тяжестью гастроинтестинальных симптомов [4]. Тем не менее большинство авторов расценивают висцеральную гиперчувствительность как биологический маркер СРК, а баллонный тест – как специфичный (95 %) и чувствительный (70 %) метод диагностики СРК, а также оценки эффективности лекарственных препаратов при их клинических испытаниях [5].
С помощью позитронной эмиссионной томографии было показано, что в ответ на проведение баллонного теста у здоровых лиц отмечается активация передней части ободка перешейка коры. Эта зона лимбической системы связана с активными опиатными соединениями, что, возможно, в норме обеспечивает снижение восприятия входящих болевых стимулов. У больных СРК активируются другие отделы коры головного мозга, особенно префронтальная зона, которая не связана с опиатами. Предполагается, что при СРК нарушен процесс нисходящего подавления восприятия боли, т.е. имеется центральная антиноцицептивная дисфункция [6]. Возникла гипотеза, объясняющая возникновение абдоминальной боли при СРК нарушением контроля ЦНС над восходящими болевыми импульсами [7].
Полагают, что в генезе висцеральной гиперчувствительности и нарушенной моторики при СРК ведущую роль может играть вовлечение в этот процесс серотонинергических механизмов [8]. Серотонинергическая система мозга участвует в регуляции общего уровня активности ЦНС, двигательной активности, сна и памяти, в существенной степени определяет эмоциональное поведение человека [9]. Несмотря на значительное разнообразие серотониновых рецепторов, в серотонинергической системе головного мозга и желудочно-кишечном тракте определяются сходные рецепторные типы. В кишечнике образуется 80 % серотонина организма, и источником его в значительной мере является кишечная микробиота.
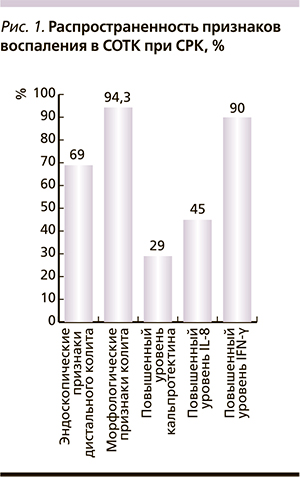 Исследования последних лет характеризуют СРК как заболевание, сопровождаемое изменениями микроэкологического статуса толстой кишки. Способность индигенной кишечной микрофлоры вырабатывать нейротрансмиттеры, влияющие на ЦНС и тем самым изменяющие секрецию, моторику кишечника и порог висцеральной чувствительности, свидетельствует о важности дисбиотических изменений при СРК [10]. К настоящему времени получены убедительные доказательства того, что микрофлора кишечника больных СРК существенно отличается от таковой здоровых лиц [11]. A. Kassinen и соавт. [12] обнаружили существенные различия в содержании некоторых родов бактерий в разных библиотеках клонов, что подтверждено методом количественной полимеразной цепной реакции филотипов родов Coprococcus, Collinsella и Coprobacillus. По данным отечественных авторов, результаты микробиологического анализа микрофлоры толстой кишки при СРК свидетельствуют о существенном снижении бифидо-, лактобактерий, энтерококков. У 30–85 % больных СРК, согласно разным источникам, был обнаружен синдром избыточного бактериального роста (СИБР) [13]. Развившийся по той или иной причине СИБР инициирует воспалительный ответ, который в свою очередь усиливает клинические проявления кишечных дисфункций. Синдром избыточного бактериального роста может быть одной из причин развития микроскопического воспаления слизистой оболочки кишечника [14].
Исследования последних лет характеризуют СРК как заболевание, сопровождаемое изменениями микроэкологического статуса толстой кишки. Способность индигенной кишечной микрофлоры вырабатывать нейротрансмиттеры, влияющие на ЦНС и тем самым изменяющие секрецию, моторику кишечника и порог висцеральной чувствительности, свидетельствует о важности дисбиотических изменений при СРК [10]. К настоящему времени получены убедительные доказательства того, что микрофлора кишечника больных СРК существенно отличается от таковой здоровых лиц [11]. A. Kassinen и соавт. [12] обнаружили существенные различия в содержании некоторых родов бактерий в разных библиотеках клонов, что подтверждено методом количественной полимеразной цепной реакции филотипов родов Coprococcus, Collinsella и Coprobacillus. По данным отечественных авторов, результаты микробиологического анализа микрофлоры толстой кишки при СРК свидетельствуют о существенном снижении бифидо-, лактобактерий, энтерококков. У 30–85 % больных СРК, согласно разным источникам, был обнаружен синдром избыточного бактериального роста (СИБР) [13]. Развившийся по той или иной причине СИБР инициирует воспалительный ответ, который в свою очередь усиливает клинические проявления кишечных дисфункций. Синдром избыточного бактериального роста может быть одной из причин развития микроскопического воспаления слизистой оболочки кишечника [14].
Кишечная микрофлора в результате жизнедеятельности может образовывать свободные (деконъюгированные) желчные кислоты, гидроксиды жирных кислот, бактериальные токсины, протеазы и различные метаболиты (фенолы, биогенные амины и др.), влияющие на моторику кишечника и состояние его рецепторного аппарата [15]. У пациентов с СРК снижена концентрация как отдельных, так и суммарных короткоцепочечных жирных кислот. Кроме то...












