Кардиология №10 / 2013
Роль генетических факторов в прогнозировании осложнений на протяжении года после инфаркта миокарда
ФГБУ НИИ комплексных проблем сердечно-сосудистых заболеваний СО РАМН, 650002 Кемерово, Сосновый бульвар, 6; ФГБУ НИИ медицинской генетики СО РАМН; ООО «Геномная диагностика»
Изучена выборка из 165 больных инфарктом миокарда (ИМ) с подъемом сегмента ST в отношении прогнозирования риска развития осложнений в течение года (рецидив нефатального ИМ или смерть). При анализе 32 полиморфных генетических вариантов с доказанной ролью в патогенезе различных сердечно-сосудистых заболеваний показано, что наилучшая модель стратификации пациентов с ИМ по риску осложнений включала варианты rs4291 (А-240Т) гена ACE, rs6025 (G1691A, лейденская мутация) гена F5 и rs5918 (Leu59Pro) гена IGTB3. Значение C-статистики для генетической модели составило 0,75 (0,64; 0,86) при р=0,001, что сравнимо с показателями шкалы GRACE для этой же группы пациентов: 0,73 (0,61; 0,85). Таким образом, показано, что анализ небольшого числа генетических маркеров достаточен для построения модели оценки риска развития осложнений ИМ, сравнимой по прогностической значимости с подходами, используемыми в настоящее время в клинической практике. Для подтверждения клинической ценности полученная модель должна быть апробирована на независимых выборках пациентов с ИМ. При анализе ассоциаций индивидуальных генетических маркеров с «конечными точками» показано, что носительство аллеля Т (генотипы АТ и ТТ) по варианту rs4291 гена АСЕ и генотип СG по варианту rs328 гена LPL являются факторами риска смерти в течение года после ИМ; лейденская мутация (rs6025) гена F5 связана с высоким риском развития повторного нефатального ИМ/смерти в течение года после ИМ; генотип СС полиморфного варианта rs10811661, располагающегося в локусе 9р21, оказывает протективный эффект в отношении рецидива ИМ/смерти в течение года.
В настоящее время смертность и инвалидность от осложнений инфаркта миокарда (ИМ) остаются высокими, что определяет необходимость повышения эффективности прогнозирования неблагоприятного течения заболевания. Доказано, что пациентам с высоким риском развития осложнений требуется дорогостоящее лечение, тогда как в группе с низким риском лечение может быть более избирательным, что позволяет более эффективно распределять ресурсы общества [1].
Одной из наиболее простых и получивших широкое распространение систем оценки риска развития осложнений ИМ является индекс TIMI Risk Score-STEMI [2]. Данный метод позволяет оценить вероятность летального исхода ИМ в течение 30 дней от начала заболевания у пациентов, подвергшихся тромболитической терапии (ТЛТ). Это единственная шкала стратификации риска, одобренная Российским кардиологическим обществом для практического применения у больных ИМ с подъемом сегмента ST (ИМпST). Несмотря на простоту использования, она обладает достаточной высокой прогностической ценностью — площадь под ROC-кривой при использовании данной системы на целевой выборке пациентов составляет 0,78 [2].
Относительно недавно в кардиологическую практику вошла шкала GRACE (Global Registry of Acute Coronary Events) [3], построенная с использование выборки, включающей 43 810 пациентов. Данная модель продемонстрировала хорошие прогностические возможности: показатель С-статистики в отношении стратификации риска смерти в течение 6 мес составил 0,81, а госпитальной летальности — 0,82, что подтвердилось при проверке данной модели на базе данных регистра GUSTO IIb [3]. Данная модель — единственная, которая позволяет оценить риск не только смерти, но и рецидива нефатального ИМ, и применима для всех больных вне зависимости от метода реперфузии миокарда. С целью определения степени индивидуального риска по шкале GRACE разработана программа, on-line версия которой представлена на сайте http://www.outcomes.org.
Несмотря на существование нескольких альтернативных способов оценки риска развития осложнений ИМ, для практикующего врача остается открытым вопрос о выборе наиболее чувствительного и специфичного из них. Кроме того, необходимо наличие возможности выбора прогностического подхода в зависимости от демографических, социальных и экономических условий конкретной популяции. Недостатком существующих методов является также и то, что они не учитывают генетические факторы, которые играют важную роль в структуре подверженности сердечно-сосудистым осложнениям (ССО) [4] и остаются постоянными на протяжении жизни, т.е. их оценка возможна на любом этапе, в том числе задолго до манифестации заболевания (предиктивное тестирование).
В исследовании S.E. Humphries и соавт. [5] получены доказательства того, что система оценки риска развития ССО в общей популяции, включающая наряду с традиционными факторами риска (ФР) набор нескольких генотипов, была более эффективна, чем система, основанная исключительно на традиционных ФР. Работа была выполнена с использованием данных Northwick Park Heart study II (Великобритания), где наблюдение проводилось за выборкой, включающей 3052 мужчин среднего возраста, за 10-летний период было зафиксировано 250 коронарных осложнений. Точность диагностики традиционной системы оценки риска и оценки риска, основанной исключительно на генетических маркерах, оказались сопоставимыми, а комбинация генетических и традиционных ФР улучшала показатель системы примерно на 10%.
Кроме того, получены данные о том, что генетические маркеры могут повышать прогностическую способность шкал, предназначенных для прогнозирования риска развития осложнений ИМ. Включение в модель GRACE информации о генотипе по полиморфному варианту rs1333049, расположенному в локусе хромосомы 9р21, позволяло улучшить ее прогностическую значимость на 5,9% и тем самым точнее предсказывать принадлежность пациентов к той или иной группе риска развития повторного ИМ/ смерти [6].
Целями настоящего исследования являлись построение модели оценки риска развития осложнений ИМ, основанной на анализе полиморфных генетических вариантов генов-кандидатов сердечно-сосудистых заболеваний (ССЗ) и анализ ассоциаций индивидуальных генетических маркеров со статусом пациентов через 12 мес после острого заболевания.
Материал и методы
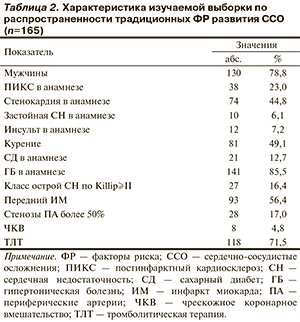 В исследование включены 165 пациентов, госпитализированных в Кемеровский кардиологический диспансер по поводу острого коронарного синдрома с подъемом сегмента ST давностью менее 24 ч. Алгоритм обследования включал сбор жалоб, анамнеза, клинический осмотр кардиологом, запись электрокардиограммы, оценку уровня кардиоспецифических ферментов, контроль показателей системной гемодинамики, проведение эхокардиографии. Всем пациентам в кратчайшие сроки определяли предпочтительный метод реперфузии миокарда — чрескожное коронарное вмешате...
В исследование включены 165 пациентов, госпитализированных в Кемеровский кардиологический диспансер по поводу острого коронарного синдрома с подъемом сегмента ST давностью менее 24 ч. Алгоритм обследования включал сбор жалоб, анамнеза, клинический осмотр кардиологом, запись электрокардиограммы, оценку уровня кардиоспецифических ферментов, контроль показателей системной гемодинамики, проведение эхокардиографии. Всем пациентам в кратчайшие сроки определяли предпочтительный метод реперфузии миокарда — чрескожное коронарное вмешате...













