Акушерство и Гинекология №5 / 2019
Роль рецепторов NOD1 и NOD2 в распознавании патогенов в женском репродуктивном тракте
1) ФГАОУ ВО «Белгородский государственный национальный исследовательский университет», г. Белгород, Россия;
2) ФГБОУ ВО «Воронежский государственный университет», г. Воронеж, Россия
Рецепторы NOD1 и NOD2 относятся к семейству NOD-подобных рецепторов (NOD-like receptors, NLRs). Они являются цитозольными рецепторами клеток врожденного иммунитета, распознающими компоненты пептидогликана бактерий и РНК вирусов. NOD1 и NOD2 экспрессируются во всех органах женского репродуктивного тракта, при этом максимальная их экспрессия наблюдается в маточных трубах. Экспрессия мРНК NOD1 в эндометрии не зависит от фазы менструльного цикла, в то время как экспрессия NOD2 максимальна в позднюю секреторную фазу. NOD1 и NOD2 способны распознавать ряд условно-патогенных и патогенных бактерий, а также вирусов и простейших. Некоторые микроорганизмы (Listeria monocytogenes, Neisseria gonorrhoeae) имеют механизмы, позволяющие избегать распознавания, что обеспечивает их длительную внутриклеточную персистенцию.
Уникальность женского репродуктивного тракта заключается в его способности одновременно выполнять функцию защиты от патогенов и обеспечивать иммунологическую толерантность к сперматозоидам и наполовину чужеродному плоду [1].
Система врожденного иммунитета, которая является первой линией иммунной защиты, осуществляет распознавание патогенных микроорганизмов с помощью сигнальных рецепторов. Роль Толл-подобных рецепторов в патогенезе репродуктивных осложнений наиболее изучена [2]. Однако недавно были открыты и другие группы сигнальных рецепторов, среди которых наибольший интерес представляют NOD-подобные рецепторы.
NOD-подобные рецепторы (NOD-like receptors, NLRs) – это семейство рецепторов, состоящее из 23 структурно родственных белков [3], играющих важную роль в индукции иммунного ответа и апоптоза, а также в процессе развития зиготы [4].
NLRs разделяют на группы в зависимости от их структуры и биологических функций в организме человека.
К группе рецепторов, играющих роль в процессах репродукции, относят NLRP 2, 4, 5, 8, 9, 11, 13 и 14 [5]. Показана их важная роль в развитии зиготы на стадии морулы, в патогенезе трофобластической болезни и болезней геномного импринтинга (синдрома Беквита-Видемана и Сильвера-Рассела) [4, 5].
Большая группа NLRs индуцирует воспалительный ответ. NLRP1, NLRC4 и NLRP3 участвуют в образовании инфламмасом [6, 7]. Функции NLRP6, NLRP7 и NLRP12 изучены недостаточно хорошо, однако предполагают, что они способны играть роль в образовании инфламмасом, а также ингибировать NF-kB-зависимую продукцию цитокинов [8–10].
Рецепторы NOD1 и NOD2 не участвуют в образовании инфламмасом, но при связывании с пептидогликаном бактерий и вирусной РНК индуцируют выработку провоспалительных цитокинов, интерферонов, а также активируют процессы аутофагии [5]. Данные рецепторы представлены во всех отделах женского репродуктивного тракта.
Рецепторы NOD1 и NOD2. Рецепторы NOD1 (синонимы: NLRC1, CARD4) и NOD2 (синонимы: NLRC2, CARD15), как и остальные члены семейства NLRs, являются цитоплазменными рецепторами системы врожденного иммунитета [11]. Есть данные, что NOD1 и NOD2 могут перемещаться на клеточную мембрану, к месту бактериальной инвазии [12]. NOD1 экспрессируется, как гемопоэтическими, так и негемопоэтическими клетками, NOD2 – гемопоэтичскими и некоторыми эпителиальными клетками [13, 14].
Активация NOD1 происходит при связывании c диаминопимелиновой кислотой (iE-DAP), являющейся частью пептидогликана всех грамотрицательных и некоторых грамположительных бактерий. NOD2 связывается c мурамилпептидом, который является основной структурной единицей пептидогликана и входит в состав клеточной стенки, как грамположительных, так и грамотрицательных бактерий [12].
Основные сигнальные пути рецепторов NOD1 и NOD2 представлены на рисунке.
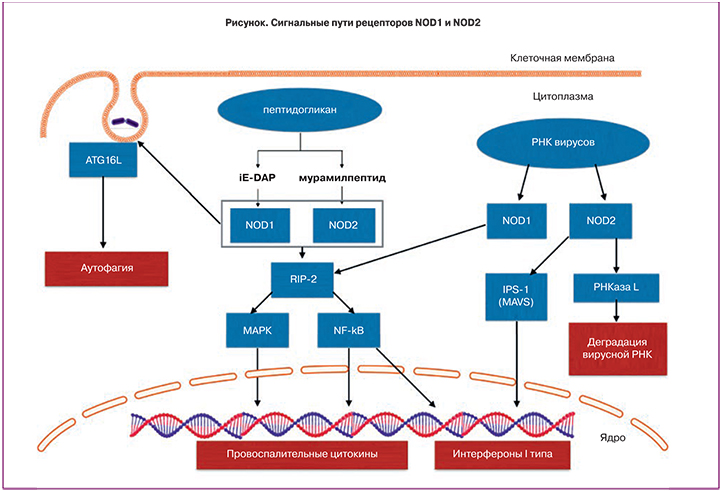
Связывание NOD1 и NOD2 c компонентами пептидогликана приводит к выработке антимикробных пептидов, провоспалительных цитокинов и хемокинов [13].
NOD1 и NOD2 способны распознавать вирусную РНК, что приводит к стимуляции выработки и...












