Урология №3 (supplement) / 2017
Симптомы нижних мочевыводящих путей вследствие доброкачественной гиперплазии предстательной железы в 2017 г.: обновления 32-го съезда Европейской ассоциации урологов
2-е урологическое отделение ГБУЗ ГКБ им. Д. Д. Плетнева ДЗ г. Москвы, кафедра урологии и андрологии ФГБУ ГНЦ ФМБЦ им. А. И. Бурназяна ФМБА РФ, Москва, Россия
В обзоре литературы обобщены новые данные о монотерапии и комбинированном лечении симптомов нижних мочевыводящих путей (СНМП) у мужчин с доброкачественной гиперплазией простаты (ДГПЖ). Отдельное внимание уделено докладам, прозвучавшим на 32-м Конгрессе Европейской ассоциации урологов и опубликованным в сборнике абстрактов данного конгресса. Приведены новые данные об эпидемиологии СНМП вследствие ДГПЖ, отражены последние изменения в патогенезе возникновения симптомов, приведен критический анализ последних публикаций по вопросам консервативной терапии α-адреноблокаторами, ингибиторами 5α-редуктазы, м-холиноблокаторами, а также ингибиторами фосфодиэстеразы 5-го типа. Проанализированы последние данные по эффективности хирургических методов лечения ДГПЖ.
В марте 2017 г. в Лондоне (Великобритания) прошел очередной, 32-й съезд Европейской ассоциации урологов. Проблема симптомов нижних мочевыводящих путей (СНМП) вследствие доброкачественной гиперплазии предстательной железы (ДГПЖ) традиционно являлась одной из наиболее часто обсуждаемых тем. Данному вопросу были посвящены одна пленарная, одна тематическая сессия и одна видеосессия. Наиболее новые сведения за последние годы были доложены на четырех постерных сессиях, которые затрагивали помимо вопросов консервативного и оперативного лечения еще и ряд спорных и неизученных вопросов этиологии, патогенеза и прогрессирования СНМП, отдельное внимание было уделено вопросам эпидемиологии СНМП.
В настоящем обзоре будут подробно освещены новые тенденции, спорные вопросы по данной проблематике. Поскольку после 31-го Европейского урологического конгресса также был написан аналогичный обзор, представляется актуальным проведение тех или иных параллелей с анализом перспектив развития каждого конкретного направления.
Начиная разбирать и анализировать новые данные по этиологии и патогенезу заболевания, нельзя не остановиться на работе [1], в которой были представлены новые данные, свидетельствующие о нейроэндокринной этиологии ДГПЖ. Авторами были проведены исследования на мышах, которые показали, что снижение периферического синтеза серотонина приводит к развитию фиброзной гиперплазии стромы предстательной железы посредством стимуляции андрогенных рецепторов. Подавление выработки серотонина в переходной зоне простаты может сопровождаться развитием гиперплазии последней. Прогрессирование заболевания характеризуется дальнейшим угнетением синтеза серотонина в тканях простаты. Одним из важных терапевтических подходов терапии СНМП в будущем может стать разработка препаратов, позволяющих нормализовать обмен серотонина в тканях простаты, что может быть реализировано путем либо стимуляции рецепторов серотонина, либо медикаментозного увеличения его концентрации в тканях простаты [1].
Новые данные об эпидемиологии СНМП у корейских мужчин были приведены в работе Y. Park и соавт. [2]. Авторы обследовали более 11 тыс. корейских мужчин старше 40 лет. Выполнялось трансректальное УЗИ предстательной железы и расширенное биохимическое обследование крови. Основной задачей исследования стало обнаружение возможных биохимических отклонений у пациентов с факторами риска прогрессирования заболевания (показатель IPSS более 8 баллов, объем простаты более 30 см3).
Средняя скорость увеличения объема простаты в год в исследуемой когорте составила 0,48 см3 в год. Выявлено, что при повышении уровня α-фетопротеина риск прогрессирования заболевания увеличивается, подобной зависимости не было выявлено ни для липидов высокой плотности, ни для печеночных трансаминаз и уровня азотистых шлаков крови [2].
S. Kim и соавт. [3] изучили сократимость гладкомышечной мускулатуры шейки мочевого пузыря и простатического отдела уретры в эксперименте. Релаксация гладких мышц шейки мочевого пузыря происходила как при воздействии тамсулозина, так и при использовании силденафила. Относительно новыми фактами можно считать то, что величина эффекта зависела от возраста и объема гиперплазированной ткани, т.е. теоретически эффективность α-адреноблокаторов и ингибиторов фосфодиэстеразы 5-типа может быть более высокой для пожилых пациентов с большим объемом простаты, чем для относительно молодых больных без выраженного увеличения предстательной железы [3].
Еще один возможный из терапевтических подходов к терапии СНМП был изучен в работе [4]. Авторами был уточнен механизм релаксации гладких мышц шейки мочевого пузыря под воздействием пикотамида. В эксперименте сокращение гладких мышц вызывалось воздействием эндотелина, последний cпособствует мышечному спазму путем стимуляции как непосредственно эндотелиновых рецепторов, так и через α-адренэргические механизмы и путем активации рецепторов тромбоксана. Установлено, что пикотамид, ингибитор α-адренорецепторов и рецепторов тромбоксана, вызывает более сильную релаксацию, чем просто блокирование α-адренорецепторов. Результатом последующих работ по изучению блокаторов рецепторов тромбоксана может стать разработка новых лекарственных препаратов для терапии СНМП.
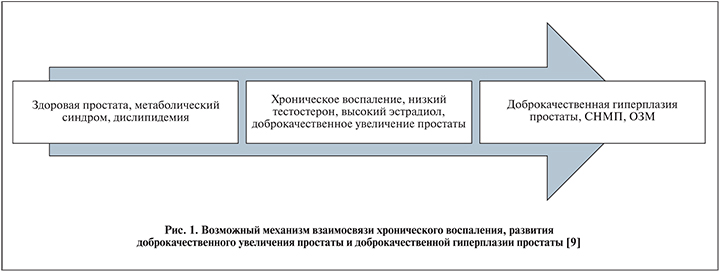
Как и на прошлогоднем конгрессе Европейской урологической ассоциации было представлено несколько работ, посвященных изучению дефектов протекания воспалительного процесса в тканях предстательной железы в виде нарушения аутофагоцитоза; считается, что послед...












