Терапия №3 / 2019
Сосудистые когнитивные нарушения: расширение терапевтических возможностей
Кафедра нервных болезней Института профессионального образования ФГАУО ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России
Сосудистые когнитивные нарушения представляют собой большую проблему в современной клинической практике, однако наши терапевтические возможности остаются довольно ограниченными, так как молекулярные и клеточные механизмы, лежащие в основе цереброваскулярных болезней, до сих пор недостаточно изучены. Лечение усложняется сосуществованием сосудистой и нейродегенеративной патологии: у пациентов с деменцией обычно встречаются вместе болезнь Альцгеймера (БА) и сосудистая деменция (СД). До сих пор научные исследования деменции в основном были сосредоточены либо на амилоидной, либо на сосудистой патологии. Несмотря на интенсивную работу ученых, этот подход не дал результатов в плане лечения. Существует мнение, что успех может обеспечить только комбинированная фармакотерапия деменции.
Когнитивные расстройства после инсульта и/или сердечно-сосудистых эпизодов чрезвычайно распространены даже в случае успешного клинического выздоровления после кардиоваскулярных заболеваний. СД является одной из деменций, при которой возможна профилактика с воздействием на модифицируемые «сосудистые» факторы риска. Управление ими значительно уменьшит вероятность развития СД в дальнейшей жизни.
В ближайшем будущем по мере углубленного изучения когнитивных процессов и механизмов их повреждения будут создаваться новые, таргетные препараты против деменции. Кроме того, многообещающей стратегией борьбы с деменцией можно считать фармакологические меры по усилению церебрального резерва через имитацию когнитивного отдыха. Правильный терапевтический подход может остановить или даже обратить прогрессирование умеренных когнитивных расстройств до деменции и в конечном итоге задержать и предотвратить сосудистые и другие деменции, включая БА.
Сосудистая деменция (СД) – необратимое состояние, связанное в основном с различными цереброваскулярными заболеваниями (гипоперфузия, гипоксия, ишемия и инсульт), для которых характерно прогрессирующее ухудшение когнитивных функций и проблемы с социальной адаптацией. Как известно, деменция относится к возраст-зависимым состояниям, и общемировая тенденция к старению населения ведет к прогрессирующему увеличению заболеваемости. По оценкам ВОЗ, к 2050 г. численность населения, страдающего деменцией, утроится и превысит 100 млн. СД является вторым наиболее распространенным типом деменции после болезни Альцгеймера (БА) и составляет около 15% от общего количества ее случаев [1].
МКБ-10 определяет СД (F01) как деменцию, которая возникает после цереброваскулярных заболеваний. Ее наиболее характерными клиническими проявлениями служат нарушения внимания и исполнительных функций, умеренные нарушения памяти, трудности при выполнения многоэтапных задач, замедленное мышление, уменьшенные способности планирования, рассуждения, решения проблем, нарушается активность повседневной жизни [2, 3].
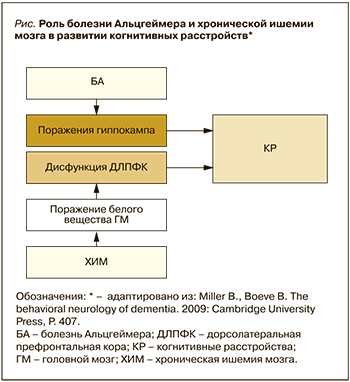 При постановке диагноза СД необходимо помнить о возможности клинического сосуществования СД и БА (так называемые смешанные когнитивные расстройства) и о том, что хроническая ишемия мозга (ХИМ), возникающая при любых цереброваскулярных заболеваниях (ЦВБ), может стимулировать развитие субклинически существующего нейродегенеративного процесса (например, БА) или значительно ухудшать уже имеющиеся когнитивные нарушения [4, 5] (рис.). Около 40% пациентов с БА имеют некоторые формы сосудистых когнитивных нарушений и деменции [6]. С другой стороны, амилоидная патология способствует страданию мелких сосудов и уменьшает кровоток через суженные сосуды [7]. Кроме того, надо учитывать, что, хотя СД часто рассматривается как один тип нарушений памяти, на самом деле существуют различные его подтипы, неодинаковые по клинической картине [8–12].
При постановке диагноза СД необходимо помнить о возможности клинического сосуществования СД и БА (так называемые смешанные когнитивные расстройства) и о том, что хроническая ишемия мозга (ХИМ), возникающая при любых цереброваскулярных заболеваниях (ЦВБ), может стимулировать развитие субклинически существующего нейродегенеративного процесса (например, БА) или значительно ухудшать уже имеющиеся когнитивные нарушения [4, 5] (рис.). Около 40% пациентов с БА имеют некоторые формы сосудистых когнитивных нарушений и деменции [6]. С другой стороны, амилоидная патология способствует страданию мелких сосудов и уменьшает кровоток через суженные сосуды [7]. Кроме того, надо учитывать, что, хотя СД часто рассматривается как один тип нарушений памяти, на самом деле существуют различные его подтипы, неодинаковые по клинической картине [8–12].
МКБ-10 выделяет следующие подгруппы СД:
- СД с острым началом (F01.0);
- мультиинфарктная деменция (F01.1);
- подкорковая СД (F01.2);
- смешанная корковая и подкорковая СД (F01.3);
- другая СД (F01.8);
- СД неуточненная (F01.9).
ЦВБ часто начинаются исподволь и прогрессируют постепенно. На ранней стадии выделяют умеренные когнитивные расстройства (УКР), при которых наблюдается когнитивное снижение, выходящее за рамки возрастной нормы, но не приводящее к утрате независимости в повседневной жизни. Для описания УКР сосудистого происхождения P. Sachdev в 1999 г. впервые предложил термин «сосудистые когнитивные расстройства» (СКР) [13]. СКР подразумевает когнитивный дефицит по крайней мере в одной когнитивной области без нарушения повседневной активности [14]. При СД напротив, имеются нарушения двух или более когнитивных функций, приводящие к снижению повседневной активности.
ДИАГНОСТИКА СОСУДИСТЫХ КОГНИТИВНЫХ НАРУШЕНИЙ
Диагностика СКР и СД включает оценку когнитивных функций и поведенческих симптомов, сбор анамнеза; кроме этого, обязательно учитываются показатели нейровизуализации.
Хотя в арсенале современной медицины есть различные клинические диагностические инструменты [15, 16] и критерии СД, такие как NINDS-AIREN [17], DSM-IV [18], ADDTC [19], разработка единых критериев до сих пор вызывает затруднения.
При исследовании когнитивных функций в рамках диагностики СКР и СД прежде всего оцениваются:
- исполнительные функции (планирование и внимание);
- речь (импрессивная и экспрессивная);
- память (заучивание и воспоминание);
- визуально-пространственные навыки (способность иметь дело с невербальной, графической или географической информацией);
- активность повседневной жизнедеятельности (шкала ADL).
Поведенческие и эмоциональные расстройства часто возникают при сосудистой патологии. Например, так называемая сосудистая депрессия (депрессия у пожилого человека с ЦВБ) возникает более чем у половины пациентов с ЦВБ. Синдром характеризуется ярко выраженной фронто-стриатной лимбической дисфункцией. У таких больных в большей степени, чем у пациентов с «несосудистой» депрессией, выражены апатия, психомоторная заторможенность, нарушение повседневной деятельности, снижение понимания, в меньшей степени – волнение и чувство вины. Также у них отмечается более слабый, замедленный и нестабильный ответ на терапию антидепрессантами, при этом они лучше реагируют на лечение основного сосудистого заболевания. Эти наблюдения легли в основу гипотезы «сосудистой депрессии», в соответствии с которой ЦВБ могут предрасполагать, ускорять или усугублять некоторые гериатрические синдромы депрессии.
При диагностике сосудистых УКР и СД первостепенное значение имеют данные анамнеза:
- наличие сердечно-сосудистых факторов риска (неконтролируемая гипертензия, диабет и др.);
- данные магнитно-резонансной томографии (МРТ) в пользу наличия церебральных инсультов (диффузная гиперинтенсивность белого вещества, очаги гиперинтенсив...












