Урология №5 / 2024
Современные оптические неинвазивные технологии в диагностике урологических заболеваний. Обзор литературы. Часть I
1) СПб ГБУЗ «Клиническая больница Святителя Луки», Санкт-Петербург, Россия;
2) ЧОУВО «Санкт-Петербургский медико-социальный институт», Санкт-Петербург, Россия;
3) ФГБОУ ВО «Санкт-Петербургский государственный университет», Санкт-Петербург, Россия;
4) ФГБОУ ВО «Орловский государственный университет им. И. С. Тургенева», Орел, Россия;
5) ФГБУ «Научно-исследовательский институт гриппа им. А. А. Смородинцева», Санкт-Петербург, Россия;
6) ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России, Санкт-Петербург, Россия
Эффекты взаимодействия оптического излучения и биологических тканей лежат в основе различных технологий оптической диагностики – лазерной допплеровской флоуметрии, спектроскопии диффузного отражения, флуоресцентной спектроскопии, фотодинамической диагностики (флуоресцентной цистоскопии), конфокальной микроскопии, оптической когерентной томографии и др. Результативность применения данных технологий является предметом изучения в разных областях медицины – дерматологии и офтальмологии, анестезиологии и кардиохирургии, при диагностике злокачественных новообразований и др.
В первой части нашего обзора были рассмотрены и систематизированы имеющиеся данные о целесообразности использования в качестве диагностического инструмента лазерной допплеровской флоуметрии и спектроскопии диффузного отражения в урологической практике.
Постоянный поиск новых и усовершенствование уже имеющихся диагностических технологий являются одним из важнейших условий повышения качества медицинской помощи [1]. При этом особой ценностью отличаются такие методы диагностики, которые сочетают, с одной стороны, высокую информативность, чувствительность и специфичность, с другой, быстроту, динамичность и возможность практически немедленного получения результатов в режиме реального времени, с третьей,минимальную инвазивность или в идеале полное отсутствие таковой. С этих позиций весьма перспективными представляются оптические методы выявления повреждений внутренней среды на органном, тканевом, клеточном и молекулярном уровнях [2].
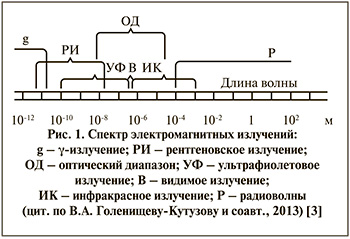
Все методы оптической диагностики базируются на эффектах взаимодействия оптического излучения и биологических тканей. Оптическое излучение представляет собой электромагнитные волны, диапазон длин которых ограничен с одной стороны ультрафиолетовой (УФ) частью спектра, с другой – инфракрасной (ИК). Как показано на рис. 1, длина волн непосредственно оптического диапазона (видимой части спектра) составляет 0,40–0,76 мкм, УФ-диапазона – 0,18–0,40 мкм, ИК-диапазона – 0,76–2000 мкм [3].
После поглощения оптического излучения одна часть световой энергии преобразуется в тепловую, другая расходуется на фотохимические реакции, третья поглощается хромофорами с дальнейшим испусканием кванта света с бо́льшей длиной волны. Данный феномен получил название «люминесценции», две ее разновидности – «флуоресценция» и «фосфоресценция» – различаются длительностью свечения и энергией излучаемых фотонов.
Оптические характеристики биологических тканей определяют те или иные хромофоры – ненасыщенные атомарные группы в составе молекулы, способные поглощать свет с определенной длиной волны и за счет этого обеспечивать цвет соединения. К хромофорам относятся, например, меланин, гемоглобин, билирубин и др. [4, 5].
Хромофоры со способностью к флуоресценции – флуорофоры – в различных тканях имеют разные спектральные области поглощения и флуоресценции, различные квантовые выходы флуоресценции, различные времена затухания флуоресценции. Атомарные группировки со свойствами флуорофоров присутствуют в составе гемоглобина и оксигемоглобина, коллагена и эластина, меланина, триптофана и триптофан-содержащих белков, пиридоксина, липоферментов, флавинов, порфиринов, окисленных и восстановленных форм внутриклеточных никотинамидных коферментов НАДН (никотинамидадениндинуклеотид) и НАДФН (никотинамидадениндинуклеотидфосфат) и др. [6–10].
В настоящее время среди различных диагностических оптических технологий внимание исследователей прежде всего привлекают такие методы диагностики, как лазерная допплеровская флоуметрия, спектроскопия диффузного отражения, флуоресцентная спектроскопия, фотодинамическая диагностика, конфокальная микроскопия, оптическая когерентная томография [11–13].
Лазерная допплеровская флоуметрия (ЛДФ) представляет собой современный неинвазивный оптический метод изучения особенностей движения крови по сосудам микроциркуляторного русла (сосуды с диаметром от 2 до 200 мкм), выявления нарушений микроциркуляции крови (артериальная и венозная гиперемии, ишемия, стаз), анализа состояния механизмов регуляции тонуса микрососудов (нейрогенного, миогенного, эндотелиального, дыхательного, сердечного) [14].
Клиническая значимость метода ЛДФ обусловлена тем, что все нарушения регионарного кровотока и микроциркуляции как типовые патологические процессы являются фрагментом патогенеза чрезвычайного множества заболеваний и/или их осложнений, в т.ч. урологического профиля, например, таких, как доброкачественная гиперплазия предстательной железы, гиперактивный мочевой пузырь, посттравматические стриктуры уретры [15].
В основе метода ЛДФ лежит эффект Допплера, суть которого заключается в изменении частоты и, соответственно, длины волны колебаний, воспринимаемых наблюдателем (преемником) при движении источника колебаний и наблюдателем относительно друг друга [16]. Эффект Допплера возникает при отражении зондирующего лазерного луча от подвижных биологических структур – циркулирующих в крови эритроцитов. Разность между частотами зондирующего и отраженного лучей получила название допплеровского сдвига частоты. Допплеровский сдвиг частоты является количественной величиной (обозначается символом ∆f) и, как видно из уравнения Δf=2nV/λ, прямо пропорционален скорости движения эритроцитов (V) и показател...












