Акушерство и Гинекология №11 / 2024
Современные тренды в коррекции симптомов генитоуринарного менопаузального синдрома: роль андрогенов
ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России, Москва, Россия
Генитоуринарный менопаузальный синдром (ГУМС) обычно наблюдается у женщин в период пери- и постменопаузы и характеризуется большим разнообразием симптомов, возникающих в результате атрофических изменений вульвы, влагалища (ВВА) и нижних мочевыводящих путей. Популяционные исследования показали крайне негативное влияние мочеполовых симптомов на качество жизни женщин, их эмоциональное состояние, сексуальную активность и самооценку. В нескольких работах продемонстрирована тесная связь между сексуальной дисфункцией и симптомами, связанными с ГУМС. ГУМС/ВВА – это хроническое заболевание, симптомы которого прогрессируют со временем, приводя к функциональным и анатомическим изменениям в органах малого таза. Своевременно назначенное лечение может уменьшить тяжесть клинических проявлений, предотвратить прогрессирование заболевания и развитие осложнений, а также улучшить качество жизни женщин. На протяжении многих лет локальная терапия эстрогенами считается золотым стандартом для лечения симптомов ГУМС/ВВА. Но, учитывая современную концепцию патогенеза ГУМС о том, что не только дефицит эстрогенов, но и снижение продукции андрогенов с возрастом способствует развитию мочеполовых симптомов, применение локального ДГЭА (дегидроэпиандростерона) (прастерона) является новым трендом в коррекции ГУМС и сексуальной дисфункции у женщин в постменопаузе. Многочисленные рандомизированные клинические исследования показали высокую эффективность локального прастерона в отношении субъективных симптомов и объективных признаков ВВА, а также повышения либидо и сексуальной функции в целом по сравнению с плацебо. Данные эффекты реализуются благодаря специфическому внутриклеточному метаболизму ДГЭА в активные эстрогены и андрогены согласно механизмам современной интракринологии. Полученные данные о высокой безопасности локального прастерона позволяют использовать препарат «Интрароса» в течение длительного времени у пациенток в постменопаузе, в том числе в возрасте старше 60 лет.
Заключение: В данном литературном обзоре приведены современные сведения об эпидемиологии, патогенезе и методах лечения ГУМС. Приведены данные рандомизированных клинических исследований об эффективности и безопасности интравагинального ДГЭА (прастерона) и даны объяснения эффектов данного гормона в отношении симптомов и признаков ГУМС с точки зрения механизмов науки интракринологии.
Вклад авторов: Ермакова Е.И., Сметник А.А., Табеева Г.И. – концепция и дизайн, сбор и обработка материала, написание текста, редактирование.
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Работа выполнена без спонсорской поддержки.
Для цитирования: Ермакова Е.И., Сметник А.А., Табеева Г.И. Современные тренды в коррекции симптомов генитоуринарного менопаузального синдрома: роль андрогенов.
Акушерство и гинекология. 2024; 11: 207-214
https://dx.doi.org/10.18565/aig.2024.284
Генитоуринарный менопаузальный синдром (ГУМС) – симптомокомплекс, ассоциированный со снижением уровней эстрогенов и других половых стероидов, включающий изменения, возникающие в наружных половых органах, промежности, влагалище, уретре и мочевом пузыре [1, 2]. Данный термин был утвержден комиссиями Североамериканского общества по менопаузе (NAMS) и Международного общества по изучению сексуального здоровья женщин (ISSWSH) в 2014 г. [1], а в 2015 г. одобрен Российской Ассоциацией по менопаузе. По мнению экспертов, в отличие от ранее применяемых понятий «вульвовагинальная атрофия» (ВВА) и «атрофический вагинит» термин «ГУМС» представляется с медицинской точки зрения более точным, емким и приемлемым для клиницистов, исследователей, преподавателей, пациенток и средств массовой информации [1, 2]. ВВА является одним из компонентов ГУМС.
Согласно позиции NAMS 2020 г., симптомы ГУМС/ВВА наблюдаются у 15–25% женщин в перименопаузе и 50–84% женщин в постменопаузе [3].
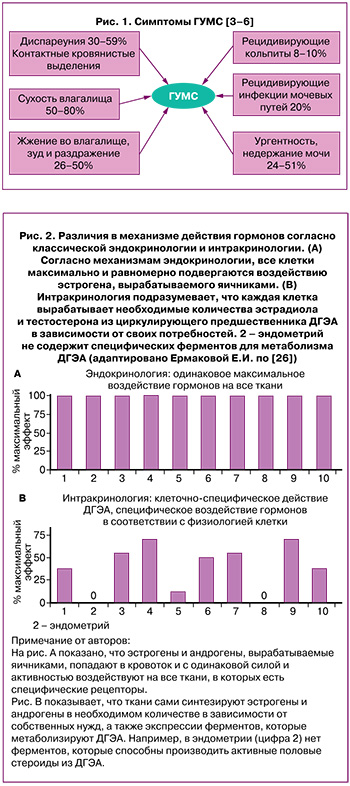
ГУМС включает вагинальные проявления, нарушения мочеиспускания и сексуальные расстройства, развивающиеся на фоне дефицита половых гормонов (рис. 1). К возможным вторичным изменениям и заболеваниям половых органов относят: атрофию половых губ, опущение стенок влагалища, выпадение тазовых органов с развитием обструктивного мочеиспускания [3–5].
В нескольких исследованиях оценивалось влияние проявлений ГУМС на качество жизни женщин, их эмоциональное благополучие и сексуальную активность. Международный опрос Women’s Voices включал 4246 европейских женщин в постменопаузе, 52% из которых сообщили о негативном влиянии ГУМС на сексуальную жизнь. При этом треть опрошенных отметили, что вагинальные симптомы влияют на самооценку и заставляют их «чувствовать себя старыми» [7]. Результаты другого популяционного исследования, включающего женщин в постменопаузе, показали, что мочеполовые симптомы отрицательно влияли на интерес к сексу (59%), отношения с партнером (55%), настроение (42%), уверенность в себе и самооценку (34%) [8]. Популяционные исследования свидетельствуют о том, что многие женщины в пери- и постменопаузе молчат о своих проблемах, связанных с ГУМС, и не обращаются за помощью к врачу по разным причинам: из-за смущения и чувства стыда, убеждения в том, что данные симптомы являются нормальной частью старения, или недостатка знаний и информации в этой области [7, 9]. В связи с вышеизложенным акушерам-гинекологам необходимо активно расспрашивать женщин о наличии мочеполовых симптомов и обращать внимание на объективные проявления ГУМС/ВВА [10]:
- сухость, истончение эпителия;
- уменьшение складчатости влагалища;
- побледнение эпителия;
- наличие петехиальных кровоизлияний, признаков воспаления;
- потеря упругости тканей, подкожной жировой клетчатки;
- уменьшение количества лобковых волос;
- повышение влагалищного pH (выше 5,0).
Ключевая роль в обеспечении здоровья урогенитального тракта отводится эстрогенам, поскольку они обеспечивают пролиферацию и созревание влагалищного эпителия, повышают его секреторную активность, поддерживают кислую среду во влагалище, нормализуют микробиоценоз и увеличивают рост субэпителиальных капилляров [11, 12]. Поэтому в ответ на снижение уровня эстрогенов в пери- и постменопаузе в слизистой влагалища, вульвы, мочевого тракта, связочном аппарате малого таза развиваются ишемия и атрофические изменения [11].
Ряд публикаций свидетельствует о значимом влиянии дефицита андрогенов на развитие менопаузальных мочеполовых симптомов. Рецепторы к андрогенам экспрессируются во всех структурах урогенитального тракта, особенно интенсивно – в гладкомышечной ткани и преддверии влагалища [13]. Андрогены повышают количество и компактность коллагеновых волокон в собственной пластине, увеличивают содержание гладкомышечных волокон в стенке влагалища, регулируют секрецию муцина во влагалище, а также плотность нервных волокон и нейротрансмиссию [14]. Вышеуказанные эффекты андрогенов подтверждаются результатами экспериментальных исследований [15]. Так, в работе Cellai I. et al. подгруппам крыс после овариоэктомии вводили 17β-эстрадиол, тестостерон или тестостерон+летрозол и сравнивали их с группой интактных животных. Иммуногистохимический анализ биоптатов стенки влагалища показал, что дефицит половых стероидов после овариоэктомии индуцировал структурную атрофию эпителия и гладких мышц. Последующее введение тестостерона и тестостерона+летрозол увеличивали содержание и организацию мышечных пучков, не влияя на эпителий, в то время как 17β-эстрадиол оказывал влияние только на состояние эпителия влагалища. Кроме того, овариоэктомия приводила к снижению чувствительности к ацетилхолину и повышению чувствительности к норадреналину, что вызывало констрикцию гладкой мускулатуры. Тестостерон восстанавливал чувствительность к ацетилхолину и улучшал NO-опосредованн...












