Урология №5 / 2016
Стеноз везикоуретрального анастомоза и недержание мочи после радикальной простатэктомии: взаимосвязь и влияние на качество жизни пациентов до и после эндоскопической коррекции
Кафедра урологии ГБУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ (зав. каф. – главный уролог МЗ РФ,
д.м.н., проф. Д. Ю. Пушкарь), Москва
Введение. Рак предстательной железы (РПЖ) является наиболее распространенным злокачественным новообразованием у мужчин, которое в странах Европы и США опережает по заболеваемости рак легких и колоректальный рак [1, 2]. Так, по данным как Европейской, так и Американской ассоциаций урологов, в течение жизни диагноз РПЖ будет поставлен каждому 7-му мужчине. При этом у 80% заболевших будет диагностирован локализованный РПЖ (стадии T1–2N0M0). Ситуация в России, к сожалению, значительно хуже, и на начальные стадии РПЖ приходится лишь 50% случаев [3]. Общепринятый метод лечения локализованного РПЖ в настоящее время – это радикальная простатэктомия (РПЭ), которая в идеале является излечивающей процедурой, практически не снижающей качество жизни пациента.
Помимо онкологического результата зачастую не менее важным для пациентов является и функциональный результат операции. Под функциональным результатом подразумевается сохранение эректильной функции, удержания мочи и нормального акта мочеиспускания. При выполнении РПЭ возможно повреждение структур, ответственных за удержание мочи (шейка мочевого пузыря, мышцы промежности, мембранозный отдел уретры), что может стать причиной стрессового недержания мочи (СНМ) у 6–8% пациентов. Данное осложнение существенно снижает качество жизни пациентов [4]. Другим тяжелым осложнением РПЭ может стать развитие обструктивного мочеиспускания (инфравезикальной обструкции) или острой задержки мочи, вызванной стенозом везикоуретрального анастомоза (СВУА). В свою очередь обструктивное мочеиспускание может стать причиной развития рецидивирующей инфекции мочевыводящих путей. Послеоперационное СНМ и СВУА не являются изолированными патологиями, а зачастую встречаются в комбинации, оказывая выраженное негативное влияние на здоровье и качество жизни пациентов, и, разумеется, наносят значимый экономической ущерб, обусловленный затратами на лечение [5, 6].
В своей работе мы решили оценить частоту, степень сопутствующего СНМ и качество жизни до и после эндоскопической коррекции везикоуретрального анастомоза (ВУА) у пациентов, перенесших радикальное оперативное лечение по поводу РПЖ, а также оценить эффективность первичной и повторных эндоскопических коррекций ВУА; проследить влияние количества перенесенных эндоскопических коррекций на степень СНМ и качество жизни пациентов.
Материалы и методы. Первым этапом проведен ретроспективный анализ количества и вида (открытая позадилонная или лапароскопическая роботассистированная) РПЭ, выполненных в клинике с января 2010 по декабрь 2015 г.
Далее проведен архивный поиск и анализ историй болезней пациентов, обратившихся в нашу клинику с 2010 по 2015 г. в связи с обструктивной симптоматикой и ранее перенесших в клинике РПЭ.

В исследование были включены пациенты с обструктивной симптоматикой, обусловленной СВУА, в последующем перенесшие эндоскопическую коррекцию ВУА. Критерии исключения: наличие у пациента стриктуры уретры в отсутствие признаков стенозирования ВУА; перенесенная отрытая реконструкция ВУА.
В ходе архивного поиска собирались данные о симультанных манипуляциях; количестве и типе перенесенных каждым пациентом эндоскопических коррекций ВУА.
Следующим шагом осуществлен телефонный опрос пациентов, обратившихся в клинику в связи со СВУА.
В ходе опроса собрана следующая информация:
- наличие и степень выраженности СНМ непосредственно после РПЭ и после эндоскопической коррекции ВУА; выраженность СНМ оценивали по количеству урологических прокладок, используемых пациентами в течение суток;
- оценка качества жизни (по шкале QoL) до и после эндоскопической коррекции СВУА;
- превалирующий фактор при оценке качества жизни до и после эндоскопической коррекции ВУА: стрессовое недержание мочи или обструктивная симптоматика;
- наличие на момент опроса обструктивной симптоматики.
На заключительном этапе работы выполнена статистическая обработка полученных результатов с расчетом параметров вариационных рядов (взвешенное среднее значение, среднеквадратическое отклонение [σ], коэффициент вариации [Cv]), применением парного и непарного t-критериев Стьюдента, коэффициента корреляции Пирсона. Статистически значимыми считали различия при р<0,05.
Результаты. В период с 2010 по 2015 г. в нашей клинике было выполнено 1453 РПЭ, при этом зарегистрировано 60 случаев СВУА. Эндоскопическая коррекция ВУА выполнялась пятью хирургами (табл. 1).
Стоит отметить, что тенденция к ежегодному увеличению абсолютного числа случаев СВУА (исключение составляет 2015 г., по-видимому, из-за сравнительно малого времени, прошедшего с момента радикальной операции) пропорционально увеличению выполняемых нами простатэктомий (рис. 1). Заболеваемость СВУА после РПЭ в разные годы варьировала от 2,19 до 6,47% (рис. 2).
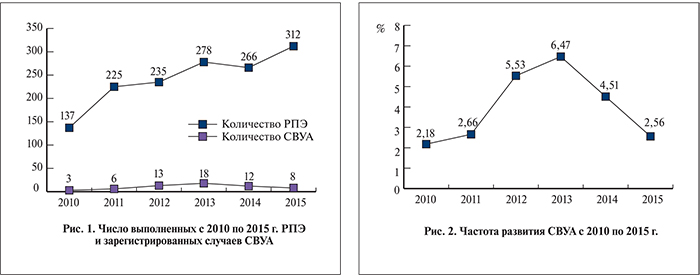
В подавляющем большинстве случаев СВУА развивались после РППЭ – 88% наблюд...












