Клиническая Нефрология №1 / 2014
Стратификация риска развития хронической болезни почек с помощью анкетирования
ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова» Минздрава России, Москва; Филиал по медицинской профилактике ГАУЗМО «Клинический центр восстановительной медицины и реабилитации», Москва; ФУВ ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, Москва
Цель. Определение частоты повышенной альбуминурии (АУ) как маркера хронической болезни почек (ХБП), выявление факторов ее развития и разработка метода расчета риска ХБП среди условно здорового населения.
Материал и методы. Обследовали 1623 человека: 390 (24 %) мужчин, 1233 (76 %) женщины; средний возраст –
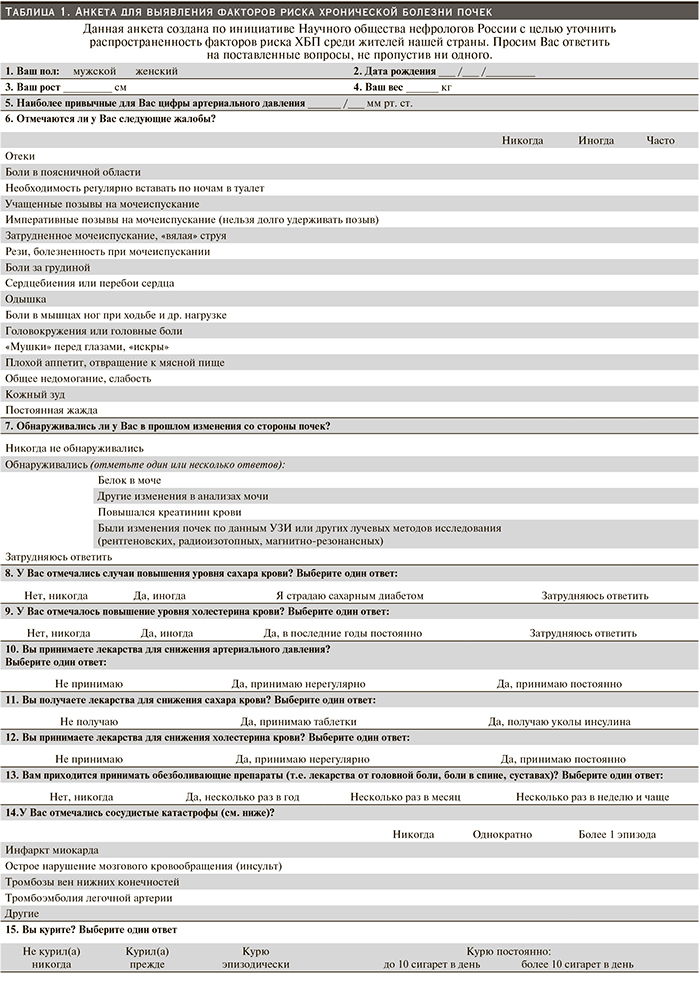
46 ± 16 лет. Всем обследуемым проводили анализы мочи с помощью тест-полосок. Уровень АУ > 30 мг/л расценивали как высокий. Для оценки возможных факторов риска ХБП нами была разработана анкета, отражающая пол, возраст, антропометрические данные пациентов, наличие сопутствующих заболеваний, приверженность здоровому образу жизни, курение. Использовался многофакторный регрессионный анализ для определения расчета риска АУ > 30 мг/л.
Результаты. АУ > 30 мг/л отмечалась более чем у 40 % лиц, обратившихся в центры здоровья. По результатам анкетирования среди жалоб, ассоциированных с АУ > 30 мг/л, чаще всего встречались таковые на отеки, боли за грудиной, плохой аппетит, отвращение к мясной пище, постоянную жажду. Частота АУ > 30 мг/л у лиц с артериальной гипертонией составила 51 %. При наличии сахарного диабета или эпизодов повышения тощаковой гликемии в анамнезе частота АУ > 30 мг/л составила 65,5 %. У лиц с избыточной массой тела и ожирением АУ >
30 мг/л была выявлена в 44 и 49 % случаев соответственно. АУ > 30 мг/л встречалась достоверно чаще у лиц, злоупотребляющих анальгетиками, с большим стажем курения, а также у лиц с малоподвижным образом жизни. Создана модель, наиболее достоверно предсказывающая развитие АУ > 30 мг/л и содержащая переменные, имеющие самостоятельное прогностическое значение.
Заключение. Риск развития ХБП среди условно здорового населения и определение показаний к нефрологическому обследованию могут оцениваться с помощью специальных анкет.
Введение
Хроническая болезнь почек (ХБП) занимает особое место среди хронических неинфекционных болезней, поскольку она широко распространена, связана с резким ухудшением качества жизни и высокой смертностью [1–3]. По данным эпидемиологических исследований, распространенность ХБП среди взрослого населения США, Западной Европы, Австралии, Китая находится в диапазоне от 11 до 16 % [4–7]. Данные о распространенности ХБП среди населения России отсут-ствуют, поскольку не проводилось соответствующих крупных популяционных исследований. Однако исследования, выполненные в отдельных категориях населения, позволяют предполагать, что распространенность ХБП в нашей стране очень высока. Так, по данным обследования пожилых пациентов, наблюдавшихся в городской поликлинике № 107 Москвы в 2008 г., у лиц старше 60 лет признаки ХБП отмечались в половине случаев, а в более старших возрастных группах – у 66,3 % [9]. Среди пациентов трудоспособного возраста, проходивших обследование в отделениях терапии Коломенской ЦРБ, частота ХБП, которая диагностировалась по наличию снижения скорости клубочковой фильтрации (СКФ), составляла 16 %, а у лиц, страдающих сердечно-сосудистыми заболеваниями, – 26 % [10]. Признаки ХБП отмечаются более чем у трети больных хронической сердечной недостаточностью [11].
Верхушку «айсберга» ХБП, привлекающую наибольшее внимание медицинского сообщества и организаторов здравоохранения, составляют больные терминальной почечной недостаточностью (ТПН), характеризующейся высокой смертностью и коморбидностью, требующей дорогостоящей заместительной почечной терапии (ЗПТ) – диализа или трансплантации почки [12–14]. В нашей стране с 1998 по 2007 г. число людей, получавших ЗПТ, увеличилось в 2,5 раза, однако и сейчас обеспеченность населения данными видами лечения остается в 3–7 раз ниже, чем в странах Евросоюза, в 10 раз ниже, чем в США [15]. Однако успешное решение проблемы ХБП путем только развития ЗПТ невозможно. Первостепенное значение имеют раннее выявление ХБП и своевременное назначение нефропротективной терапии, а также проведение комплекса профилактических мероприятий среди лиц, входящих в группу риска [16].

Диагностика ХБП строится на двух критериях: наличии маркеров почечного повреждения, среди которых ведущее место занимает повышенная альбуминурия (АУ), и/или снижение СКФ [8]. Повышение уровня АУ служит наиболее ранним и чувствительным маркером почечного повреждения и может наблюдаться даже при полном отсутствии протеинурии [17]. Ранние стадии ХБП (1 и 2) характеризуются нормальным или незначительным снижением СКФ и повышенной АУ [17, 18], которая имеет в данном случае решающее значение для диагностики. При СКФ ниже 60 мл/мин/1,73 м2 уровень АУ не имеет решающего значения для диагностики ХБП, однако он сохраняет свою роль в прогнозировании скорости прогрессирования ХБП и развития сердечно-сосудистых осложнений [19]. Более того, все шире высказывается мнение, будто изолированное (т.е. без повышения АУ) снижение СКФ в пределах 45–59 мл/мин/1,73 м2, особенно у пожилых, не требует вмешательства, поскольку из-за очень низких темпов дальнейшего падения функции почек ожидаемое время развития ТПН у них значительно превосходит ожидаемую продолжительность жизни [20].
Таким образом, исследование АУ имеет первостепенное значение для ранней диагностики ХБП, когда отсутствуют протеинурия и снижение СКФ, а также для оценки риска ее прогрессирования и развития сердечно-сосудистых осложнений – как на ранних, так и на более поздних стадиях. Простота и доступность метода – его важное достоинство, необходимое для проведения скрининговых исследований.
В настоящее время широко обсуждается, какой уровень АУ считать нормальным, поскольку и при ее значениях ниже 30 мг/г, прежде считавшихся нормальными, сохраняется корреляция между величиной АУ и риском сердечно-сосудистых осложнений [17]. Поэтому на сегодняшний день нормальным считают уровень АУ ниже 10 мг/г, а ее величину 10–29 мг/г определяют как незначительное или начальное повышение. Уровень АУ, превышающий 30 мг/г, является безусловным отклонением от нормы, маркером ХБП и фактором риска ее прогрессирования [17].
Действующие клинические рекомендации предписывают регулярное определение уровня АУ у пациентов, длительно страдающих сахарным диабетом, гипертонической болезнью [17]. Однако даже в этих группах, находящихся под пристальным наблюдением специалистов-эндокринологов и кардиологов, на практике мониторинг маркеров ХБП не всегда проводится должным образом. Лица, не страдающие данными заболеваниями, но имеющие другие факторы риска ХБП, вообще не получают внимания.
Cкрининг всего населения на предмет наличия повышенной АУ считается нерациональным из-за организационных трудностей и огромных финансовых затрат [21], поэтому представляется актуальной разработка методики, позволяющей проводить разносторонний и комплексный анализ всей совокупности факторов риска ХБП и выделять группу лиц, нуждающихся в проведении теста на АУ в первоочередном порядке.












