Терапия №8 (18) / 2017
Таурин в комплексной терапии больных хронической сердечной недостаточностью
1 ФГБОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова», кафедра госпитальной терапии № 1 лечебного факультета, г. Москва;
2 МБУЗ «Городская клиническая больница № 15 им. О.М. Филатова», г. Москва
Включение в стандартную терапию больных ишемической болезнью сердца с хронической сердечной недостаточностью таурина в суточной дозе 750 мг снижает функциональный класс сердечной недостаточности, количество повторных госпитализаций в связи с декомпенсацией недостаточности кровообращения, но не влияет на общую летальность в течение 1 года. На фоне приема препарата улучшается диастолическая функция левого желудочка без значимой динамики размеров левых камер сердца, фракции выброса. Эффективность таурина в лечении больных подтверждается достоверным снижением в крови биомаркеров NT-proBNP и галектина-3.
Хроническая сердечная недостаточность (ХСН) осложняет течение различных заболеваний сердечно-сосудистой системы, что сопровождается ростом числа больных с недостаточностью кровообращения, высокой летальностью, социальной дезадаптацией пациентов. В настоящее время около 15 млн человек с ХСН насчитывается в европейских странах, 6 млн – в США, около 8 млн – в Российской Федерации [1–3]. На сегодняшний день 17–45% госпитализированных пациентов с ХСН умирают в течение 1 года наблюдения и 45–55% – в течение 5 лет, хотя имеется определенная тенденция к снижению летальности [4, 5]. Важной проблемой кардиологии остается развитие острой декомпенсации ХСН, требующей экстренной госпитализации пациентов, при этом больничная летальность достигает 8–10% [6, 7]. В течение года до 30% пациентов вновь направляются в стационар в связи с увеличением функционального класса ХСН. Лечение таких больных требует значительных финансовых затрат (26–39 млн евро на 100 млн населения в Европе), составляя 1–3% от общих расходов на здравоохранение в Северной Америке, Западной Европе и Латинской Америке [8–10].
В настоящее время разработаны принципы лечения ХСН с низкой фракцией выброса (ФВ), в меньшей степени – при сохраненной ФВ. При этом продолжается поиск новых лекарственных препаратов, повышающих качество жизни пациентов, способных уменьшить частоту повторных госпитализаций и улучшить прогноз заболевания. Одним из таких направлений является использование препаратов, способных восстанавливать нормальный метаболизм кардиомиоцитов [11]. Одним из них является таурин, клиническая эффективность которого была показана у пациентов с тяжелой ХСН, интоксикацией сердечными гликозидами, различными нарушениями сердечного ритма [12, 13]. Имеются единичные работы о влиянии таурина на диастолическую функцию миокарда левого желудочка (ЛЖ) и уровень биомаркеров, отражающих эффективность лечения и прогноз заболевания.
 Цель исследования: оценить эффективность таурина в лечении ХСН у больных ишемической болезнью сердца (ИБС), динамику диастолической функции ЛЖ, возможность предупреждения прогресcирования ремоделирования миокарда.
Цель исследования: оценить эффективность таурина в лечении ХСН у больных ишемической болезнью сердца (ИБС), динамику диастолической функции ЛЖ, возможность предупреждения прогресcирования ремоделирования миокарда.
МАТЕРИАЛЫ И МЕТОДЫ
Исследованы 117 больных ИБС, осложненной ХСН II–III функционального класса (ФК) по классификации NYHA, в возрасте от 54 до 76 лет, в том числе 50 мужчин и 67 женщин. Из них у 62 пациентов был выявлен II ФК ХСН, у 55 – III ФК ХСН. Длительность ХСН составляла от 2,5 года до 8 лет. Причиной развития застойной сердечной недостаточности послужили постинфарктный кардиосклероз (59 больных) и другие формы ИБС (58 больных). Продолжительность ИБС колебалась от 3 до 12 лет. Диагноз был установлен на основании клинической картины заболевания, анамнеза, ЭКГ, ЭХОКГ, коронароангиографии, данных определения дистанции шестиминутной ходьбы. Артериальная гипертензия была диагностирована у 78 пациентов.
Больные наблюдались в амбулаторных условиях и получали стандартную терапию ХСН, включавшую ингибиторы АПФ или блокаторы рецепторов ангиотензина II (блокаторы АТ1), блокаторы β-адренорецепторов, диуретики, аспирин. Нитраты принимали 22 пациента (19,7%), блокаторы кальциевых каналов – 14 (11,9%), статины – 94 больных (80,3%). В период наблюдения дозы лекарственных препаратов не меняли. После получения информированного согласия больные были распределены при помощи жеребьевки в две группы: 1-я группа (основная) – 73 пациента, получавшие дополнительно к рекомендуемой терапии ХСН курсовое лечение таурином 750 мг/сут: 500 мг утром + 250 мг вечером в течение 12 мес; 2-я группа (контрольная) – 44 пациента, не получавшие лечение таурином. За период наблюдения прекратили прием препарата 6 больных и умерли 3 пациента из 1-й группы; не закончили исследование 5 больных и умерли 2 пациента из 2-й, поэтому основную группу составили 64, а контрольную – 37 больных с ХСН II–III ФК.
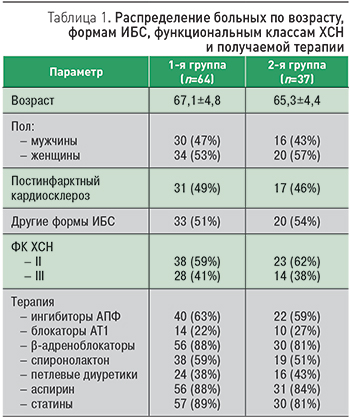
Группы пациентов были сопоставимы по возрасту, наличию сопутствующих заболеваний и принимаемой лекарственной терапии (табл. 1, 2).
Критериями исключения в нашем исследовании являлись:
- наличие злокачественных новообразований в течение последних 5 лет;
- хронические нарушения ритма и проводимости сердца (постоянная форма фибрилляции предсердий, атриовентрикулярная блокада II– III степени, устойчивая желудочковая тахикардия, полная блокада ножек пучка Гиса);
- ФВ <50%;
- детородный возраст женщин, не использующих адекватные методы контрацепции, беременность;
- гемодинамически значимое поражение клапанного аппарата сердца;
- нормальный уровень NT-proBNP (N-термальный мозговой натрийуретический пропептид);
- отсутствие согласия пациента н...












