Акушерство и Гинекология №6 / 2019
Текущий прогресс генетических и эпигенетических исследований детского церебрального паралича
1) Пекинский педиатрический научно-исследовательский институт, Пекинская Детская больница, Столичный медицинский университет, Национальный центр детского здоровья, Пекин, Китай;
2) Больница Нанфан , Южный медицинский университет, 1838 Гуанчжоу да Дао Бэй, Гунагчжоу 510515, Китай;
3) Третья прикреплённая больница, медицинский университет Гуанчжоу, 63 Дуобао Lu, Гуанчжоу, Гуандун 510150, Китай;
4) Институт фундаментальных исследований штата Нью-Йорк по инвалидности в области развития, Нью-Йорк, США
Детский церебральный паралич (ДЦП) является гетерогенным состоянием, общей чертой которого является непрогрессирующая дисфункция движения и позы. Несмотря на широкое изучение, этиология ДЦП пока не понята. Считается, что в большинстве случаев ДЦП возникает вследствие внутриутробного повреждения развивающегося мозга. Всё больше данных свидетельствуют о том, что (эпи)генетические факторы могут в сумме отвечать за большое число случаев ДЦП. В этом мини-обзоре мы сосредоточимся в основном на генетических и эпигенетических аспектах последних достижений в понимании этиологии ДЦП.
Детский церебральный паралич (ДЦП) является серьезным неонатальным дефектом и значительным экономическим и социальным бременем, который затрагивает 2-3.5 живорождений на 1 000, с распространенностью 17 000 000 по всему миру [1—6]. По данным одного из китайских исследований, распространенность ДЦП составила 2,37 на 1 000 живорожденных в провинции Хэнань [3]. Клинические характеристики ДЦП неоднородны; несмотря на различную манифестацию, общим для разных случаев является непрогрессирующая дисфункция позы и управления движением. ДЦП может быть разделен на различные неврологические подтипы на основе того, какие именно конечности поражены, а также по степени наблюдаемых двигательных нарушений: спастическая диплегия, спастическая тетраплегия, спастическая гемиплегия, дискинетический или дистонический, атаксический, гипотонический, или смешанный. На основную подгруппу — спастических (диплегических, тетраплегических или гемиплегических) ДЦП — приходится 70—80% всех случаев ДЦП [1, 2].
Эпидемиологические исследования показали, что более одной трети младенцев с ДЦП родились в результате преждевременных родов, а еще 15% имели острую энцефалопатию после своевременных родов [7, 8]. Ранее считалось, что неблагоприятные факторы внешней среды, приводящие к асфиксии в родах, являются общими факторами для развития ДЦП. В настоящее время, однако, считается, что в большинстве случаев ДЦП развивается вследствие внутриутробного повреждения развивающегося мозга, и лишь некоторые случаи обусловлены исключительно тяжелой гипоксией или ишемией в родах. Многими исследователями признано, что ДЦП обычно возникает из-за внутриутробного нарушения (пренатально) в развитии головного мозга, особенно между 24-й неделей гестации и родами. Как генезис, так и неблагоприятные перинатальные клинические условия могут вносить свой вклад в этиологию ДЦП [1, 2]. Некоторые исследования позволяют предположить, что гипоксическая ишемия или эффекты пренатальной инфекции или воспаления могут привести к общему пути перинатальной травмы головного мозга, характеризующейся нейрональной эксайтотоксичностью, апоптозом и микроглиальной активацией в критический период развития. Между тем, все большее число свидетельств указывает на то, что генетические факторы могут быть ответственными за большое количество случаев ДЦП.
В этом мини-обзоре, исследуя последние идеи и выводы о патогенезе ДЦП, мы систематически рассмотрим комплексную этиологию ДЦП, особенно гетерогенность, лежащую в основе генетических вариантов, ассоциированных с этим состоянием или являющихся его причиной.
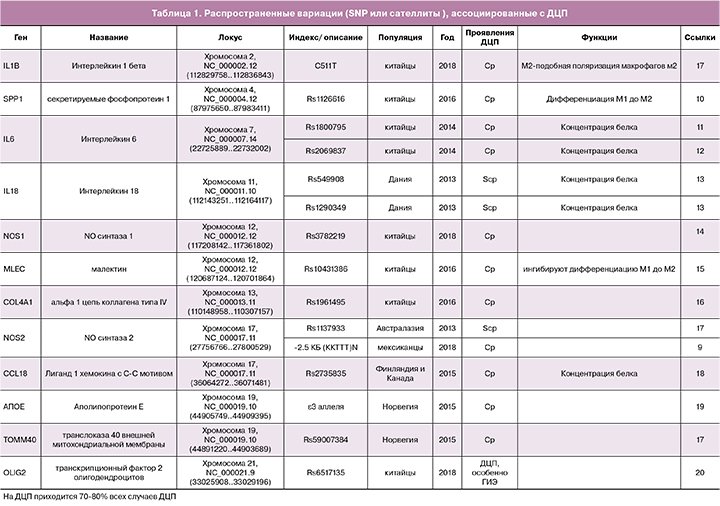
Ассоциация мутаций или изменчивости генов с ДЦП
Генетические исследования семейных и спорадических случаев ДЦП были проведены в основном для изучения изменений в уровнях последовательности ДНК. Большинство исследований генетической восприимчивости к ДЦП наиболее распространенных типов вариабельности, таких, как однонуклеотидные полиморфизмы (SNPs) и микросателлиты, проводились, как исследования ассоциаций с использованием аллель-специфичных микроматриц или масс-спектрометрии, или прямым секвенированием [9—20]. Например, Torres-Merino et al. изучали, повышается ли риск ДЦП при увеличении числа копий 2,5 тысяч пар нуклеотидов (ССТТТ)n - микросателлита в гене NOS2 и при замене C511T в промоторе гена IL-1B у пациентов с ДЦП после перинатальной гипоксическо-ишемической энцефалопатии [9]. Они обнаружили, что образованный в результате этого гаплотип (CCTTT)14/TT, может быть полезным маркером для идентификации пациентов с...












