Акушерство и Гинекология №2 / 2015
Терапия климактерического синдрома с помощью синтетического генистеина
1Женская консультация ГБУ Рязанская областная клиническая больница, Россия; 2Кафедра акушерства и гинекологии ГБОУ ВПО Рязанский государственный медицинский университет им. академика И.П. Павлова Минздрава России; 3НИО женского здоровья НИЦ ГБОУ ВПО Первый московский государственный медицинский университет им. И.М. Сеченова Минздрава России
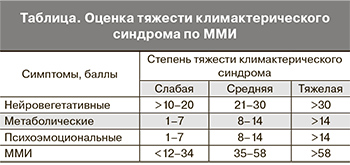
Приблизительно с 37 лет в организме женщины начинается процесс старения репродуктивной системы – прогрессирующее, необратимое угнетение биологических функций, сопровождающееся снижением фертильности. Этот инволюционный процесс доминирует в период менопаузального перехода и у значительной части женщин становится причиной приливов жара и ночной потливости, значительно снижающих качество жизни и вынуждающих обращаться за медицинской помощью [1–4]. Помимо типичных вазомоторных проявлений климактерического синдрома, женщин беспокоят разнообразные психосоматические симптомы: раздражительность, вялость, утомляемость, депрессия, головные боли, нарушение памяти, прибавка в весе, бессонница, суставные боли, сердцебиение, истерические припадки, дизурия, снижение либидо. Симптомы климактерического синдрома могут сохраняться более 15 лет после наступления менопаузы, а по мере старения женщины к ним присоединяются и поздние менопаузальные расстройства.
 Нейровегетативные проявления климактерических расстройств являются первыми и в наибольшей степени нарушающими качество жизни симптомами менопаузальных гормональных изменений. Патофизиология этих симптомов до конца не изучена. Происхождение вазомоторных жалоб (приливы жара и ночная потливость) связывают с периодическим или постоянным дефицитом эстрогенов, влияющим на способность центра терморегуляции стареющего гипоталамуса поддерживать температуру тела в нормальном диапазоне. У женщин с приливами жара границы терморегуляторной зоны сужены [5], и при этом даже незначительный выход температуры за верхний или нижний пределы данного диапазона приводит к развитию, соответственно, прилива или озноба. Большую роль в дезадаптации терморегуляции играет старение гипоталамуса, сопряженное со снижением его пластичности и нарушением обмена нейромедиаторов. В частности, с сужением терморегуляторной зоны связывают повышение содержания норадреналина и снижение серотонина в головном мозгу, но совершенно очевидно, что альтерации уровней нейрогормонов оказывают разнонаправленное действие, приводя к развитию множественных вегетативных, психических и поведенческих симптомов.
Нейровегетативные проявления климактерических расстройств являются первыми и в наибольшей степени нарушающими качество жизни симптомами менопаузальных гормональных изменений. Патофизиология этих симптомов до конца не изучена. Происхождение вазомоторных жалоб (приливы жара и ночная потливость) связывают с периодическим или постоянным дефицитом эстрогенов, влияющим на способность центра терморегуляции стареющего гипоталамуса поддерживать температуру тела в нормальном диапазоне. У женщин с приливами жара границы терморегуляторной зоны сужены [5], и при этом даже незначительный выход температуры за верхний или нижний пределы данного диапазона приводит к развитию, соответственно, прилива или озноба. Большую роль в дезадаптации терморегуляции играет старение гипоталамуса, сопряженное со снижением его пластичности и нарушением обмена нейромедиаторов. В частности, с сужением терморегуляторной зоны связывают повышение содержания норадреналина и снижение серотонина в головном мозгу, но совершенно очевидно, что альтерации уровней нейрогормонов оказывают разнонаправленное действие, приводя к развитию множественных вегетативных, психических и поведенческих симптомов.
Нет никаких сомнений, что восполнение дефицита эстрогенов является обоснованным методом лечения климактерических расстройств. Однако существование разнообразных механизмов формирования менопаузальных симптомов позволяет искать альтернативные пути улучшения качества жизни у женщин, которые не могут или, по разным причинам, не желают принимать гормональные препараты.
Изофлавоны сои широко используются в качестве альтерантивного метода лечения климактерических симптомов. Гормоноподобная активность изофлавонов описывается как селективная модуляция эстрогеновых рецепторов, объясняемая разным сродством биологически активных веществ к двум подтипам рецепторов эстрогенов (РЭ). Если афинность эстрадиола к РЭ принять за 100%, то афинность генистеина, наиболее сильного изофлавона, к РЭα составит 5%, к РЭβ – 36%, то есть в отношении РЭβ генистеин проявляет активность, сравнимую с активностью эстрона. Это делает фитоэстрогены безопасными с точки зрения избыточной пролиферации и предполагает возможность их длительного применения без прогестагенного прикрытия: низкое сродство к РЭα не позволяет фитоэстрогенам осуществить ростовые функции. Кроме того, связываясь с РЭ, фитоэстрогены блокируют взаимодействие с рецептором эндогенного эстрадиола, поэтому, будучи намного слабее эстрадиола, фитоэстрогены оказывают антиэстрогенное или эстрогенное действие в условиях, соответственно, высокой или низкой эстрогенной насыщенности, и что также позволяет относить их к разряду природных селективных модуляторов РЭ [6].
 В своей нативной форме гликозидов – соединений с сахарами – изофлавоны биологически инертны, и становятся активными только после гидролиза под действием микрофлоры кишечника и образования несахаристого компонента, так называемого агликона, обладающего эстрогенными эффектами, следовательно, зависят от состояния кишечного микроценоза. Этот факт, так же как и большие разбросы содержания изофлавонов в различных биологически активных добавках (БАД) и растительных экстрактах становится причиной противоречивых результатов клинических исследований, посвященных эффективности лечения климактерических расстройств с помощью фитоэстрогенов [7]. Синтетический генистеин, применяемый в активной форме в виде агликона в достаточной суточной дозе, может иметь преимущества перед другими видами средств, которые назначаются как альтернатива гормонам при лечении климактерических расстройств.
В своей нативной форме гликозидов – соединений с сахарами – изофлавоны биологически инертны, и становятся активными только после гидролиза под действием микрофлоры кишечника и образования несахаристого компонента, так называемого агликона, обладающего эстрогенными эффектами, следовательно, зависят от состояния кишечного микроценоза. Этот факт, так же как и большие разбросы содержания изофлавонов в различных биологически активных добавках (БАД) и растительных экстрактах становится причиной противоречивых результатов клинических исследований, посвященных эффективности лечения климактерических расстройств с помощью фитоэстрогенов [7]. Синтетический генистеин, применяемый в активной форме в виде агликона в достаточной суточной дозе, может иметь преимущества перед другими видами средств, которые назначаются как альтернатива гормонам при лечении климактерических расстройств.
Целью настоящего исследования стала оценка эффективности и безопасности синтезированного в активной форме генистеина в лечении климактерических симптомов у женщин в пери- и постменопаузе.
Материал и методы исследования
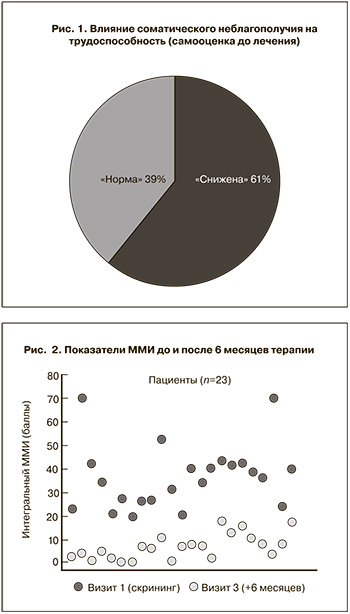
В исследование были включены 23 женщины в возрасте от 48 до 63 лет (средний возраст 55,3±3,9 года), пре...












