Фарматека №12 / 2020
Вклад аналогов соматостатина в реализацию пациенториентированного подхода к лечению акромегалии
1) Эндокринологический диспансер Департамента здравоохранения Москвы, Москва, Россия;
2) Российская медицинская академия непрерывного профессионального образования, Москва, Россия
Акромегалия является тяжелым инвалидизирующим заболеванием, курация которого требует, как правило, полидисциплинарного лечебного подхода и пожизненного приема лекарственных препаратов. Успешность длительной медикаментозной терапии зависит от эффективности и безопасности используемых препаратов. В обзоре представлены данные о современных формах медикаментозного лечения акромегалии и механизмах действия аналогов соматостатина 1-й генерации (АС1) при акромегалии. Проведен сравнительный анализ клинических исследований, касающихся эффективности и переносимости пролонгированных форм октреотида и ланреотида в качестве первичной или вторичной медикаментозной терапии. Приведены данные о приверженности пациентов длительной терапии АС1 с позиций эффективности, безопасности и переносимости фармакологических препаратов. Представлена новая форма выпуска ланреотида Аутожель, созданная при активном участии самих пациентов и медицинского персонала, имеющая очевидные преимущества перед инъекционными формами октреотидсодержащих препаратов. Описаны наиболее рациональные схемы комбинированного лечения при наличии резистентности к АС1 в зависимости рецепторного фенотипа и выраженности метаболических нарушений. По данным клинических исследований отмечена большая приверженность пациентов использованию препарата ланреотид Аутожель как в качестве монотерапии, так и в комбинации с другими препаратами.
Введение
Акромегалия представляет собой синдром, включающий различные наследственные и спорадические морфо-функциональные формы ГР (гормон роста)-секретирующих опухолей гипофиза (соматотропин), отличающиеся по степени клеточной специализации, агрессивности интракраниального роста и чувствительности к предъявляемому лечению [1, 2]. Длительная экспозиция патологической гиперсекреции ГР и его гормо-нального посредника – инсулиноподобного ростового фактора-1 (ИРФ-1) способствует активной клеточной пролиферации, подавлению апоптоза и развитию характерных для данной патологии множественных системных и обменных нарушений, негативно влияющих на продолжительность и качество жизни [3, 4]. Согласно современным международным рекомендациям, лечебная стратегия должна быть направлена на скорейшее достижение биохимической ремиссии, уменьшение тяжести системных и обменных осложнений, предотвращение (или снижение выраженности) интракраниальной компрессии [5].
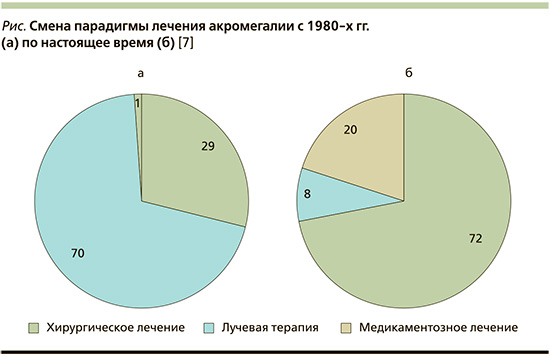
Как правило, лечение акромегалии является комплексным и в большинстве случаев требует пошагового мультидисциплинарного участия для достижения контроля заболевания. С 1980-х гг. произошли кардинальные изменения в лечебной парадигме акромегалии, проявляющиеся в существенном сокращении вклада лучевого пособия и поступательном увеличении числа больных, получающих хирургическое пособие и медикаментозную терапию. Существенное увеличение вклада фармакотерапии акромегалии произошло благодаря внедрению в клиническую практику аналогов соматостатина, доля которых среди используемых при акромегалии лекарственных препаратов (в качестве моно- и комбинированной терапии) в настоящее время составляет около 81% [6, 7].
Раздел 1
Современная методология лечения включает в приоритетной последовательности три различные модальности: транссфеноидальную хирургию, фармакотерапию и лучевое воздействие, причем, как правило, доминируют комбинированные схемы лечения (см. рисунок).
Согласно современным международным рекомендациям, приоритетным методом лечения акромегалии является эндоскопическая транссфеноидальная аденомэктомия, позволяющая быстро и с наименьшими затратами достигать контроля заболевания. Как следует из клинической практики, эффективность хирургического пособия зависит от размеров и степени инвазивности гипофизарных опухолей в кавернозный синус, квалификации нейрохирурга и оснащенности лечебного учреждения. Радикальная аденом-
эктомия, способствующая полной ремиссии акромегалии, наблюдается в 75–90% случаев при микроаденомах и в 45–70% случаев при макроаденомах гипофиза [8]. К негативным прогностическим факторам нейрохирургического вмешательства относятся молодой возраст при постановке диагноза, высокое исходное содержание ГР и ИРФ-1, большие размеры опу-холи и ускоренный ее рост, инвазию в твердую мозговую оболочку и кавернозный синус, эрозию дна турецкого седла, выявление при гистологическом исследовании слабогранулированной опухоли. Около половины прооперированных пациентов с эндоэкстраселлярными опухолями гипофиза нуждаются во вторичной медикаментозной или лучевой терапии в связи с наличием остаточной опухолевой ткани и сохраняющейся активностью заболевания [9].
Следует отметить, что даже в случае нерадикальной аденомэктомии хирургическое вмешательство представляется полезным, поскольку помимо снижения масс-эффекта и риска интракраниальной компрессии обеспечивает возможность электронно-микроскопического и иммуногистохимического исследования опухолевого материала для получения дополнительной информации относительно морфологического строения, митотической активности и рецепторного фенотипа опухоли, что является определяющим при выборе персонализированной программы вторичного лечебного пособия. Кроме того, резекция аденомы повышает эффективность последующей фармакотерапии АС1 [6, 10].
Медикаментозная терапия
На сегодняшний день известно три класса фармакологических препаратов, использующихся при лечении акромегалии (аналоги соматостатина – АС, селективные агонисты дофамина – АД, и антагонисты рецепторов ГР).
АС занимают особое место в лечении ГР-секретирующих опухолей, поскольку отличаются выраженным антисекреторным и антипролиферативным действиями. Взаимодействуя со специфическими рецепторами соматостатина в различных тканях (в т.ч. в центральной нервной системе и желудочно-кишечном тракте), АС подавляют секрецию ГР, тиреотропного гормона, а также серотонина и пептидов, продуцируемых в гастроэнтеропанкреатической эндокринной системе. Помимо антисекреторного действия АС ингибируют пролиферацию клеток путем приостановки клеточного цикла, индукции апоптоза, снижения продукции ростовых факторов и блокирования ангиогенеза, что оказывает положительное действие при ГР-продуцирующих опухолях гипофиза и различных нейроэндокринных опухолях [11, 12].
К настоящему времени накоплен достаточный опыт эффективного клинического применения АС при гипофизарной патологии, нейроэндокринных опухолях и иных нарушениях. Список нозологий, при которых успешно...












