Фарматека №7 (300) / 2015
Возможности фармакологического прекондиционирования при хирургическом лечении гемодинамически значимых стенозов сонных артерий
(1) Кафедра факультетской хирургии №1 лечебного факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава России, Москва; (2) ГКБ№1 им. Н.И. Пирогова, Москва; (3) Кафедра неврологии и нейрохирургии ФУВ ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава России, Москва; (4) Центральная клиническая больница Святителя Алексия, Москва
Статья посвящена фармакологическомупрекондиционированию к каротидной эндартерэктомии больных хронической сосудисто-мозговой недостаточностью. В основу работы положены результаты хирургического лечения 80 пациентов с гемодинамически значимым односторонним и двусторонним поражением сонных артерий. Половина этих пациентов были оперированы сразу, а другие – после фармакологического прекондиционирования препаратом Актовегин в дозе 1200 мг/сут в течение 1,5 месяца. Показано, что предоперационная подготовка еще до операции увеличивает перфузию головного мозга, определяемую посредством однофотонной эмиссионной компьютерной томографии, что значительно улучшает результаты хирургического лечения. Получена достоверная разница в когнитивной функции пациентов этих групп через 7 суток и 6 месяцев после операции. Подобное улучшение когнитивных функций коррелировало с меньшим числом асимптомныхпостпроцедуральных церебральных ишемических очагов в различных областях головного мозга. Отмечена положительная роль фармакологическогопрекондиционирования препаратом Актовегин в хирургическом лечении стенозов прецеребральных артерий, способствующего более полному восстановлению когнитивных функций.
Введение
Атеросклеротическое поражение прецеребральных артерий является одной из главных причин развития как хронических, так и острых форм мозгового кровообращения [5]. При длительно существующем окклюзионно-стенотическом процессе может возникать дискоординация тонуса сосудов головного мозга с неизбежным изменением параметров ауторегуляции.
Оперативные вмешательства, выполняемые таким больным как на сосудах головного мозга, так и на артериях других органов (коронарных, почечных, аорте, артериях нижних конечностей) с целью устранить гемодинамически значимый стеноз, сами могут приводить к колебаниям перфузионного давления не только интраоперационно, но и в послеоперационном периоде с риском возникновения гемодинамического нарушения мозгового кровообращения.
В основе развития гемодинамического нарушения мозгового крово-обращения лежит срыв функций сосудистой системы головного мозга – ауторегуляции мозгового кровообращения, способствующей минимизации отклонений гемодинамического и биохимического гомеостаза при различных физиологических и патофизиологических состояниях [7, 20]. Кроме этого существует еще один механизм повреждения клеток головного мозга при выполнении каротидной эндартерэктомии (КЭАЭ) или стентирования сонных артерий – реперфузионный синдром, характерный для всех органов при восстановлении артериального кровотока (поперечно-полосатая мускулатура конечностей, миокард и др.). Особенная опасность реперфузии при операции на сонных артериях заключается в отсутствии возможности увеличения необходимого пространства полости черепа при неизбежно возникающем отеке головного мозга. При нарушении ауторегуляции мозгового кровообращения реперфузия способна приводить не только к развитию ишемических, но и геморрагических очагов в веществе головного мозга.
Наибольший опыт борьбы с феноменом ишемии-реперфузии накоплен в кардиохирургии, где до реконструктивной операции производят различные варианты подготовки кардиомиоцитов к восстановлению артериального кровотока – прекондиционирование [2]. Пионерской при этом признается экспериментальная работа C.E. Murry и соавт. (1986), в которой авторы выполняли ишемическое прекондиционирование путем кратковременного пережатия коронарных артерий, что способствовало большей устойчивости кардиомиоцитов к последующей гипоксии [26]. В последующем такой вариант ишемического прекондиционирования был описан в некоторых работах применительно к клинической практике [27], а также предложены некоторые лекарственные средства, способные вызывать схожие эндогенные эффекты (аденозин, никорандил) [17, 21]. Следует сказать, что механическое ишемическое прекондиционирование (временное пережатие артерий головного мозга) трудновыполнимо в хирургическом лечении сосудисто-мозговой недостаточности. Кроме этого с учетом возможности развития отека головного мозга при реперфузии важно не только повышать устойчивость нейронов к гипоксии, что возможно сделать путем классического ишемического прекондиционирования, но и уменьшать проявления повреждающего на них действия атомарного кислорода при восстановлении артериального кровотока. В связи с этим оправданно применение второго вида прекондиционирования – неишемического, при котором устойчивость головного мозга к ишемии возрастает в результате предварительного воздействия различных индукторов неишемической природы, например фармакологических агентов с нейропротективными свойствами. Целью настоящей работы стала оценка возможности фармакологического прекондиционирования препаратом Актовегин при хирургическом лечении пациентов с гемодинамически значимыми стенозами прецеребральных сосудов.
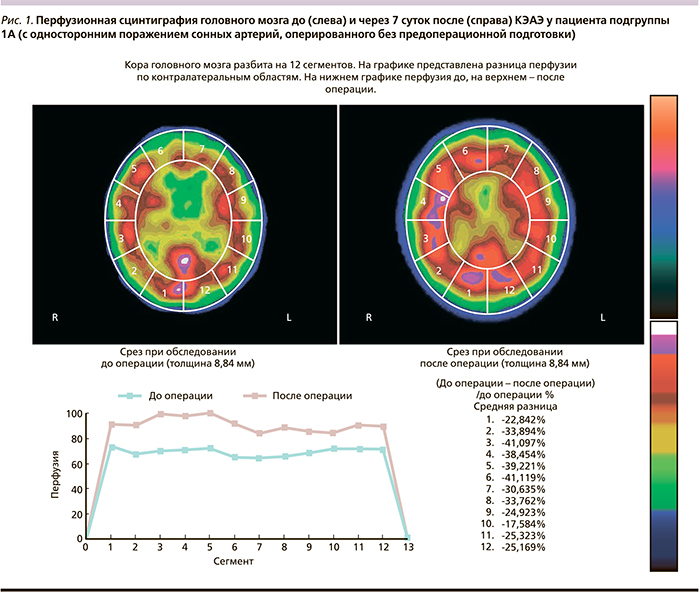
Материал и методы
В основу работы положены результаты хирургического лечения 80 пациентов (14 женщин и 66 мужчин в возрасте от 51 года до 84 лет), распределенных в две однородные группы в зависимости от тактики лечения.
Группу 1 составили 40 больных с гемодинамически значимым (более 70%) стенозом внутренней сонной артерии (подгруппа 1А – с односторонним поражением, подгруппа 1Б – с двусторонним гемодинамически значимым поражением). Пациенты этой группы были оперированы вскоре после поступления в стационар без применения предоперационного фармакологического прекондиционирования. Группа 2 также была представлена 40 пациентами с гемодинамически значимым (более 70%) стенозом внутренней сонной артерии (подгруппа 2А – с односторонним поражением, подгруппа 2Б – с двусторонним гемодинамически значимым поражением), которым перед хирургическим вмешательством проведено прекондиционирование депротеинизированным гемодериватом (Актовегин) в дозе 1200 мг/сут первые 10 дней внутривенно капельно, далее на амбулаторном этапе терапия продолжалась в таблетированной форме (по 400 мг три раза в сутки) сроком до одного месяца.
Степень сосудисто-мозговой недостаточ...












