Кардиология №12 / 2014
Взаимосвязь очагового фиброза миокарда по данным магнитно-резонансной томографии, аутоантител к рецепторам кардиомиоцитов и желудочковых нарушений ритма у больных дилатационной кардиомиопатией
ФГБУ «Российский кардиологический научно-производственный комплекс» Минздрава России , 121552, Москва, ул. 3-я Черепковская, 15а
В ходе исследования проанализированы результаты магнитно-резонансной томографии (МРТ) сердца, оценено наличие аутоантител (ауто-АТ) к β1-адренорецептору и к М2-холинорецептору у 35 больных с клиническим синдромом дилатационной кардиомиопатии (ДКМП). В сыворотке 68,6% больных ДКМП обнаруживаются ауто-АТ класса IgG к β1-адренорецептору, у 31,4% больных ауто-АТ класса IgG к М2-холинорецептору. МРТ сердца с контрастированием позволяет выявлять очаги позднего накопления гадолиния у 43% больных ДКМП. Наличие крупноочагового фиброза миокарда (очагов позднего контрастирования), по данным МРТ, наряду с выявлением ауто-АТ класса IgG к β1-адренорецептору тесно ассоциируется с наличием желудочковых нарушений ритма сердца у больных ДКМП, что позволяет использовать данные МРТ сердца, а также уровень антител к β1-адренорецептору в качестве дополнительных маркеров в определении риска желудочковых нарушений ритма у лиц с дисфункцией левого желудочка, в том числе с ДКМП.
Фатальные желудочковые аритмии по-прежнему остаются основной причиной внезапной сердечной смерти (ВСС), унося в экономически развитых странах до 2 человеческих жизней на 1000 населения в год [1]. ВСС может быть первым и единственным клиническим проявлением ишемической болезни сердца (ИБС), миокардита, гипертрофической или дилатационной кардиомиопатии (ДКМП) и других заболеваний [2, 3]. В настоящее время целый ряд клинических, инструментальных и лабораторных показателей рассматриваются в качестве предикторов желудочковых аритмий и ВСС. В этой связи многочисленные работы посвящены выявлению с помощью магнитно-резонансной томографии (МРТ) зон позднего накопления гадолиний-содержащего контрастного препарата в миокарде. Наличие таких зон ассоциировано с развитием аритмических осложнений у пациентов с дисфункцией миокарда желудочков ишемической и неишемической этиологии [3]. Выявляемым при МРТ сердца участкам позднего контрастирования соответствуют зоны некроза или фиброза миокарда, которые способны служить потенциальным субстратом для циркуляции волн re-entry при желудочковых тахикардиях (ЖТ) [4, 5]. В ряде работ продемонстрировано, что наличие рубца по данным МРТ, а также его выраженность и гетерогенность имеют значение как для возникновения спонтанных эпизодов ЖТ, так и для их индукции при проведении электрофизиологического исследования [6—8].
Согласно современным представлениям, активация аритмогенного субстрата, которым служит электрически нейтральная рубцовая зона, происходит под действием триггерных воздействий, одним из которых может быть воспаление. В современной литературе воспаление миокарда рассматривается как одно из ключевых патогенетических звеньев такого заболевания, как ДКМП. Развитие аутоиммунных реакций при этом является одним из основных механизмов, способствующих патологическому ремоделированию сердца. Большое число работ посвящено изучению роли аутоантител (ауто-АТ) к β1-адренорецептору и М2-холинорецептору в патогенезе ДКМП [9]. Частота выявления ауто-АТ к β1-адренорецептору в сыворотке больных ДКМП, по разным данным, варьирует от 26 до 60% [10, 11]. Их появление связывают с ухудшением сократительной функции миокарда левого желудочка (ЛЖ), повышением частоты развития желудочковых аритмий и более высоким риском ВСС. Экспериментальные данные свидетельствуют о способности ауто-АТ к β1-адренорецептору снижать плотность калиевых каналов кардиомиоцитов, вызывая появление ранних постдеполяризаций как потенциального триггера желудочковых аритмий [12].

Таким образом, данные литературы свидетельствуют о том, что наличие очагового фиброза миокарда является необходимым условием возникновения желудочковых аритмий. В то же время активация аутоиммунных механизмов может служить дополнительным пусковым фактором, активирующим аритмогенную зону. В связи с этим целью нашей работы была оценка возможных связей между очаговым фиброзом миокарда (по данным МРТ сердца), периферическими маркерами аутоиммунного воспаления и желудочковыми нарушениями ритма (ЖНР) у больных ДКМП.
Материал и методы
В исследование были включены 35 больных (20 мужчин и 15 женщин, средний возраст 44,2±12,1 года, группа ДКМП), данные клинико-инструментального обследования которых соответствовали клиническому диагнозу ДКМП. Диагноз ДКМП был установлен в соответствии с критериями Рабочей группы по кардиомиопатиям ВОЗ [13].
Клинико-инструментальное и лабораторное обследование включало общеклинический и биохимический анализы крови, общий анализ мочи, определение концентрации тироксина (Т4) и тиреотропного гормона в сыворотке крови, регистрацию электрокардиограммы (ЭКГ) в 12 отведениях, эхокардиографию (ЭхоКГ), суточное мониторирование ЭКГ по Холтеру, коронарографию (КГ).
У всех больных этой группы (табл. 1) регистрировались клинические проявления сердечной недостаточности, соответствующие II—IV функциональному классу по классификации NYHA. Длительность заболевания от момента клинического дебюта у пациентов группы ДКМП составила 1,25 (0,75; 3,0) года. Оценить истинную продолжительность заболевания в большинстве случаев не представлялось возможным в связи с предполагаемым протяженным по времени периодом субклинического снижения сократительной функции ЛЖ.

Результаты ЭхоКГ, проведенной у пациентов группы ДКМП, подтвердили наличие дилатированных камер сердца и снижение сократительной функции ЛЖ (конечный диастолический размер ЛЖ составил 7,1±0,8 см, конечный систолический размер ЛЖ 5,5±1,5 см, переднезадний размер правого желудочка 3,5±0,6 см, фракция выброса ЛЖ 37±11,3%). У 15 (42,9%) больных наблюдалось повышение давления в легочной артерии — в среднем 35,0 (21,5; 50) мм рт.ст.
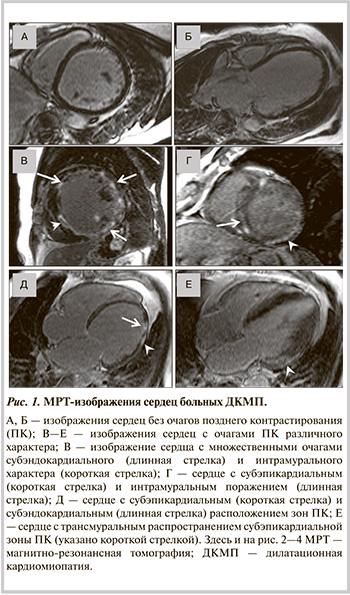 Для исключения ИБС как возможной причины расширения камер сердца всем б...
Для исключения ИБС как возможной причины расширения камер сердца всем б...












