Клиническая Нефрология №1 / 2016
Значение малобелковой диеты и назначения кетоаналогов незаменимых аминокислот для кардионефропротекции у больных хронической болезнью почек
ГБУЗ «Городская клиническая больница № 52 ДЗМ»
Малобелковые диеты (МБД) используются на протяжении многих десятилетий с целью уменьшения уремических симптомов и отсрочки заместительной почечной терапии (ЗПТ). МБД с ограничением потребления белка (0,6–0,3 г
белка/кг/сут) и назначением кетоаналогов незаменимых аминокислот (КА) рекомендуется в сочетании с другой фармакотерапией пациентам 4–5-й стадии хронической болезни почек (ХБП). Результаты исследования влияния этой диеты на скорость прогрессирования почечной недостаточности значительные и весомые, когда в качестве конечной точки исследования оценивается время начала диализа. Коррекция симптомов уремической интоксикации позволяет инициировать процедуру гемодиализа (ГД) при более низком уровне остаточной функции почек.
В большинстве случаев осложнения при ХБП связаны с сердечно-сосудистыми и метаболическими нарушениями, которые приводят к сокращению продолжительности жизни и снижению качества жизни пациентов. Строгая МБД в сочетании с назначением препаратов кетоаналогов незаменимых аминокислот позволяет предотвращать эти нарушения. Наконец, регулярный мониторинг нутритивного статуса в сочетании с назначением кетоаналогов аминокислот позволяет избегать развития его нарушений, что подтверждается отсутствием таких осложнений, влияющих на долгосрочные исходы у пациентов на додиализной стадии заболевания. Таким образом, строгая МБД в сочетании с назначением кетоаналогов незаменимых аминокислот, обладая кардионефропротективным эффектом в силу своей доступности, эффективности и безопасности заслуживает внимания как способ ведения приверженных пациентов с ХБП, позволяющий безопасно отдалить время начала диализа.
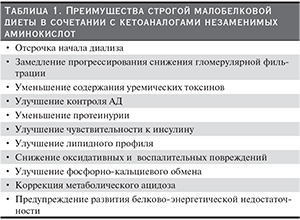
Как для нефрологов, так и для пациентов с ХБП одной из основных терапевтических целей является задержка времени до начала диализа, замедление прогрессирования почечной недостаточности за счет коррекции уремической интоксикации. При этом важной задачей при лечении пациентов с ХБП остается поддержание удовлетворительного нутритивного статуса, профилактика сердечно-сосудистых и метаболических расстройств, ухудшающих качество жизни и приводящих к сокращению продолжительности жизни больных с почечной недостаточностью. В качестве препаратов первой линии терапии для достижения некоторых из этих целей, особенно прогрессирования почечной недостаточности и сердечно-сосудистых осложнений, предлагаются ингибиторы ангиотензин-превращающего фермента (ИАПФ) и блокаторы рецепторов ангиотензина. Рекомендуется назначение МБД, которая является также синергистом для ингибиторов ренин-ангиотензин-альдостероновой системы (табл. 1).
Более 140 лет назад было показано, что снижение потребления белка благоприятно влияет на уремический синдром – преимущественно из-за уменьшения накопления продуктов метаболизма пищевого белка, а также фосфатов и снижения ацидоза. Кроме того, в последнее время было показано, что изменения количества потребляемого с пищей белка может сильно влиять на скорость потери функции почек, по крайней мере в некоторых моделях у животных [1].
Более 20 лет назад Бергстрём. и соавт. [4] подчеркнули важность влияния терапии на додиализной стадии на отдаленные исходы у пациентов с ХБП, что было подтверждено позже в других исследованиях [5].
Помимо обычной МБД, которая обеспечивает потребление 0,6–0,8 г белка/кг/сут для лечения пациентов с ХБП была предложена строгая МБД (сМБД) с очень низким содержанием белков в сочетании с назначением препаратов, содержащих незаменимые аминокислоты (ЭАК) или кальциевые соли их безазотистых кетоаналогов (KA); необходимым количеством водорастворимых витаминов, карбоната кальция и железа. Такое сочетание позволяет безопасно ограничивать суточное потребление белка до 0,3 г/кг/сут, обеспечивая достаточное количество незаменимых аминокислот и нейтральный баланс азота в связи с уменьшением азота мочевины. У больных ХБП адаптивный ответ на МБД с низким содержанием белков сохраняется длительное время [2].
Мониторинг больных, находящихся на строгой МБД в сочетании с применением кетоаналогов незаменимых аминокислот
Строгая МБД предусматривает потребление белка 0,3–0,5 г/кг/сут с высоким процентом белков растительного происхождения (табл. 2). Энергопотребление (30–35 ккал/кг/сут) обеспечивается в основном за счет углеводов (65%), липиды и белки покрывают 30 и 5% общей энергии потребления соответственно.
Преимуществом назначения препаратов, содержащих незаменимые аминокислоты и кетоаналоги незаменимых аминокислот для пациентов с ХБП, является отсутствие необходимости употребления больших количеств белка с высокой биологической ценностью, а также возможность расширить выбор продуктов с лучшими вкусовыми качествами.
При нефротическом синдроме потребление пациентами белка с пищей может быть увеличено на 1,5 г белка высокой биологической ценности на каждый грамм белка, потерянного с мочой, при протеинурии выше 3 г/сут.
Строгая МБД в сочетании с назначением кетоаналогов незаменимых аминокислот показана пациентам 4–5-й стадий ХБП без тяжелых сопутствующих заболеваний, предрасполагающих к развитию гиперкатаболического синдрома.
Пациенты, не спосбные приспособиться к такой диете и/или строгому мониторингу, также должны быть исключены.
 Такой вид диетотерапии предполагает необходимость более частых консультаций клиницистов и диетологов. Программа тщательного клинического мониторинга позволяет лучше контролировать АД и адекватность питания пациентов, а также проверять их комплаентность в отношении назначенной диетотерапии. В этих условиях строгая МБД в сочетании с назначением кетоаналогов незаменимых аминокислот может быть широко предлагаться, хотя на практике полноценно используется примерно 30–40% пациентов 4–5-й стадий ХБП.
Такой вид диетотерапии предполагает необходимость более частых консультаций клиницистов и диетологов. Программа тщательного клинического мониторинга позволяет лучше контролировать АД и адекватность питания пациентов, а также проверять их комплаентность в отношении назначенной диетотерапии. В этих условиях строгая МБД в сочетании с назначением кетоаналогов незаменимых аминокислот может быть широко предлагаться, хотя на практике полноценно используется примерно 30–40% пациентов 4–5-й стадий ХБП.
У пациентов, не имеющих осложнений, дополнительных катаболических факторов, потребление белка может быть рассчитано в соответствии с балансом азота, что равно потере азота с мочой плюс немочевая экскреция азота; последняя не зависит от потребления белка и составляет в среднем 0,031 г/кг массы тела/сут [6].
Пищевые дневники пациентов позволяют оценивать фактическое потребление энергии. Соблюдение диеты, которое является краеугольным камнем эффективности лечения, определяется как фактическое потребление, которое не должно отличаться более чем на 20% от предписанного потребления. Даже у тщательно отобранных и мотивированных пациентов удовлетворительная комплаентность достигалась лишь в 40% и 60% [7]. Исследование MDRD (Modification of Diet in Renal Disease Study) подтвердило, что степень соблюдения диеты в группе пацие...












