Урология №6 / 2025
Электромагнитная стимуляция мышц тазового дна в лечении недержания мочи после радикальной простатэктомии: результаты проспективного рандомизированного контролируемого клинического исследования
1) ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, кафедра урологии и андрологии им. акад. Н.А. Лопаткина ИХ, Москва, Россия;
2) ММКЦ «Коммунарка», Москва, Россия
Введение. Рак предстательной железы (РПЖ) остается актуальной проблемой здравоохранения с распространенностью в Российской Федерации за 2021 г. на уровне 187,3 на 100 тыс. населения. При этом наиболее часто в России РПЖ диагностируют на I и II стадиях заболевания (15,7 и 45,1% соответственно за 2021 г.) [1]. Радикальная простатэктомия (РПЭ) является одним из основных методов лечения локализованного рака предстательной железы и позволяет достичь хороших онкологических результатов. Однако данное оперативное вмешательство зачастую приводит к развитию стрессового недержания мочи (СНМ), частота которого через 12 месяцев после операции по данным разных авторов составляет 11–22% [2–5].
Согласно и отечественным, и зарубежным клиническим рекомендациям, консервативное лечение СНМ является терапией первой линии [6–8]. К методам консервативного лечения относятся упражнения для укрепления мышц тазового дна, поведенческая терапия, биологическая обратная связь, электрическая стимуляция мышц тазового дна и экстракорпоральная магнитная стимуляция [9].
Экстракорпоральная магнитная стимуляция (ЭМС) была впервые предложена для клинического применения в США в 1998 г. N.T. Galloway [10]. Электрический ток, возникающий в специальном индукторе аппарата для ЭМС, формирует импульсное магнитное поле в 2–3 Тл, которое, согласно закону электромагнитной индукции М. Фарадея, индуцирует электрический ток в проводящих структурах организма, таких как аксоны мотонейронов, вызывая их деполяризацию и запуск потенциала действия [11]. Таким образом, ЭМС является разновидностью электростимуляции, при которой магнитное поле является проводником электрического тока, в связи с чем отсутствует необходимость в наложении электродов на поверхность тела.
Терапевтический эффект ЭМС в лечении СНМ обусловлен воздействием высоких частот магнитного поля (50–100 Гц) на периферические эфферентные волокна полового нерва. В результате повышается тонус и усиливается сокращение мышц тазового дна, в том числе наружного мочевого сфинктера, который играет ключевую роль в удержании мочи у пациентов после РПЭ [12]. Преимуществами ЭМС перед другими методами консервативного лечения СНМ являются неинвазивность, безболезненность, возможность проведения процедуры в одежде, отсутствие необходимости в установке электродов, а также способность одновременно воздействовать на большое количество мышечных волокон тазового дна [13].
Цель исследования. Оценка эффективности и безопасности экстракорпоральной электромагнитной стимуляции мышц тазового дна у пациентов с недержанием мочи после радикальной простатэктомии.
Материалы и методы. В период с февраля по декабрь 2024 г. проведено проспективное контролируемое клиническое исследование эффективности и безопасности экстракорпоральной электромагнитной стимуляции мышц тазового дна у пациентов с недержанием мочи после радикальной простатэктомии на базе ММКЦ «Коммунарка» исследование было открытым – без ослепления участников и исследователей. В исследование включен 101 пациент, которые были разделены на две группы: экспериментальную (n=51) и контрольную (n=50) (рис. 1). Распределение пациентов по группам проводилось с использованием метода блочной рандомизации с блоками переменного размера (4, 6, 8) с помощью генератора случайных чисел. Размер блока выбирался случайным образом для каждого последующего блока. Последовательность распределения внутри каждого блока также определялась случайным образом.
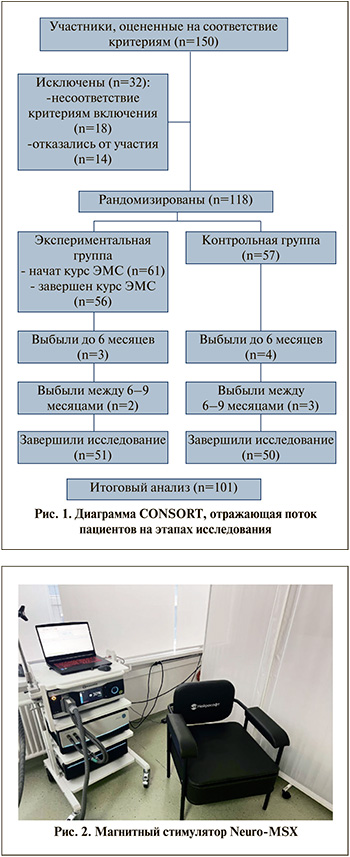
Критериями включения пациентов в исследование являлись: наличие недержания мочи через 3 месяца после радикальной простатэктомии по поводу локализованного рака предстательной железы, отсутствие биохимического рецидива РПЖ, отрицательный хирургический край по данным гистологического исследования, регулярное выполнение упражнений Кегеля и информированное согласие пациента на участие в исследовании.
Критерии исключения: наличие нейрогенных нарушений мочеиспускания, декомпенсированные соматические заболевания, наличие электронных имплантированных устройств (кардиостимуляторы и др.), металлические имплантаты в области таза, активные инфекции мочевыводящих путей, прием антихолинергических препаратов и/...












