Фарматека №9 / 2025
Проблема лекарственно-индуцированной гепатотоксичности в онкологической практике и методы ее коррекции
Волгоградский государственный медицинский университет, Волгоград, Россия
Лекарственное поражение печени представляет собой серьезную проблему в онкологической практике, обусловленную низкой селективностью противоопухолевых препаратов и их метаболитов. Рост показателей выживаемости онкологических пациентов и расширение арсенала химиотерапевтических средств, включая таргетные препараты и иммунотерапию, способствуют увеличению распространенности лекарственного поражения печени, что требует эффективных подходов к профилактике и коррекции. Обзор анализирует механизмы гепатотоксичности химиотерапевтических средств, классификации и диагностику лекарственных поражений печени.
Ведение пациентов включает мониторинг биохимии, редукцию доз химиотерапевтических средств и применение гепатопротекторов. Показано, что среди современных подходов к коррекции лекарственных поражений печени важное место занимает использование поликомпонентного препарата (Ремаксол®, МНН: Инозин+Меглюмин+Метионин+Никотинамид+Янтарная кислота). Данная фиксированная комбинация обеспечивает комплексное патогенетическое воздействие, включая коррекцию митохондриальной дисфункции, снижение оксидативного стресса, стимуляцию регенерации гепатоцитов и потенцирование детоксикационных процессов. Результаты клинических исследований демонстрируют эффективность этого препарата как для профилактики, так и для лечения лекарственных поражений печени у онкологических пациентов, получающих полихимиотерапию.
Для цитирования: Скворцов В.В., Коломыцев В.В., Горюнова Л.В. Проблема лекарственно-индуцированной гепатотоксичности в онкологической практике и методы ее коррекции. Фарматека. 2025;32(9):119-125. DOI: https://dx.doi.org/10.18565/pharmateca.2025.9.119-125
Вклад авторов: Концепция и дизайн исследования – В.В. Скворцов. Сбор и обработка материала – В.В. Коломыцев, Л.В. Горюнова. Написание текста – В.В. Коломыцев. Редактирование – В.В. Скворцов, Л.В. Горюнова.
Конфликт интересов: Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Финансирование: Работа выполнена без спонсорской поддержки.
Введение
Онкологические заболевания представляют собой одну из наиболее значимых проблем общественного здравоохранения на глобальном уровне, занимая 2-е место в структуре смертности населения. В РФ в 2024 г. диагностировано 698 693 новых случая злокачественных новообразований (ЗНО). На конец года на учете состояло 4,3 млн чел. (распространенность – 2948,6 случая на 100 тыс.) [1]. В 2023 г. от ЗНО умерли 288,8 тыс. чел. Из них 598 – от осложнений химиотерапии (ХТ) (0,2% от онкологической смертности) [1, 2]. Химиотерапевтические средства (ХТС) обладают цитостатическим и цитотоксическим действием, но их низкая селективность обуславливает поражение здоровых клеток, что проявляется целым рядом побочных эффектов, таких как лекарственно-индуцированная гепатотоксичность (ЛИГ) [3, 4].
Анализ частоты ЛИГ показывает, что повышение аланинаминотрансферазы (АЛТ)/ аспартатаминотрансферазы (АСТ) характерно для 30–70% пациентов, получающих антиметаболиты (фторурацил, гемцитабин) и алкилирующие агенты (циклофосфамид). Для противоопухолевых антибиотиков (доксорубицин) этот показатель составляет ~40%, для ингибиторов тирозинкиназ (пазопаниб, сунитиниб) – >40–50% с риском тяжелого поражения (АЛТ/АСТ >5N у 2–8% пациентов). Моноклональные антитела могут вызывать единичные случаи лекарственного поражения печени (ЛПП) вплоть до фульминантной недостаточности, в то время как тамоксифен ассоциирован с развитием метаболически ассоциированной жировой болезни печени у 4% пациентов к окончанию первого года терапии [5].
В исследовании Зукова Р.А. и соавт. было показано, что у пациентов с онкологическими заболеваниями, получающих полихимиотерапию (ПХТ), наиболее частыми режимами, сопровождающимися гепатотоксичностью, являются комбинации антиметаболитов и алкилирующих агентов (30,35% случаев), а также алкилирующих агентов с препаратами, воздействующими на тубулин (16,26%) [6].
Лекарственно-индуцированная гепатотоксичность
ЛИГ является следствием реализации гепатотоксического потенциала ХТС и при прогрессировании закономерно приводит к формированию ЛПП в срок от 5 до 90 дней от начала приема лекарственного средства (ЛС) (табл. 1) [7].
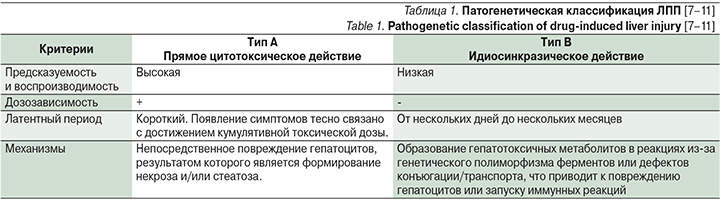
Прямая гепатотоксичность ХТС представляет собой повреждение гепатоцитов, обусловленное прямым цитотоксическим действием самих препаратов или их реактивных метаболитов. Ключевыми механизмами данного повреждения выступают индукция оксидативного стресса, ионный дисбаланс, а также прямая дестабилизация митохондриальных мембран, приводящая к энергетическому дефициту и запуску апоптоза/некроза. Важным патогенетическим звеном является и опосредованное повреждение, связанное с угнетением системы CYP. Низкая селективность ХТС приводит к подавлению детоксикационной функции гепатоцитов, что способствует кумуляции токсинов [5, 12].
В контексте развития ЛПП у онкологических пациентов необходимо учитывать не только изолированную гепатотоксичность ХТС, но и комплексный спектр эффектов, возникающих в результате их использования параллельно с другими лекарственными средствами. Это обусловлено применением в клинической практике политерапии, включающей ряд препаратов, действие которых направлено на коррекцию осложнений ХТ и лечение сопутствующей патологии, что увеличивает риск формирования нежелательных лекарственных взаимодействий (НЛВ) [5, 8].
Фармакокинетическое взаимодействие – ключевой фактор в патогенезе ЛПП. Большинство ХТС метаболизируются в печени при участии цитохрома P450 (CYP), а другие препараты могут иметь свойства его индукторов или ингибиторов, следовательно, при политерапии увеличивается риск развития НЛВ (рисунок) [8].
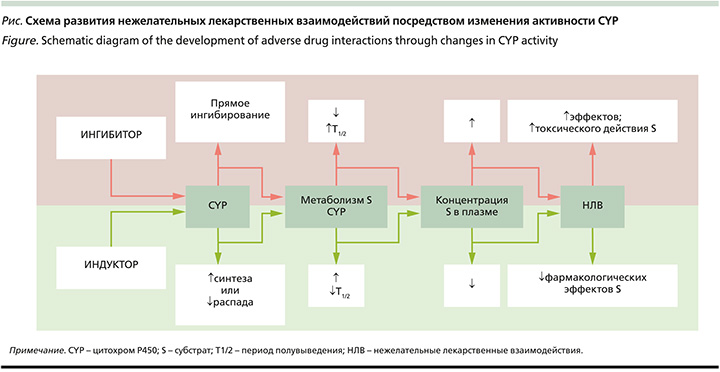
В контексте биотрансформации ЛС значимую роль играют индивидуальные (генетические) особенности пациента, которые могут способствовать развитию идиосинкразических реакций за счет измененной активности ферментов I–III фаз биотрансформации (CYP, ферменты конъюгации, транспортные системы), что определяет фармакокинетику и фармакодинамику препаратов, метаболизируемых данными ферментными комплексами [8, 13].
В дополнение к эт...












